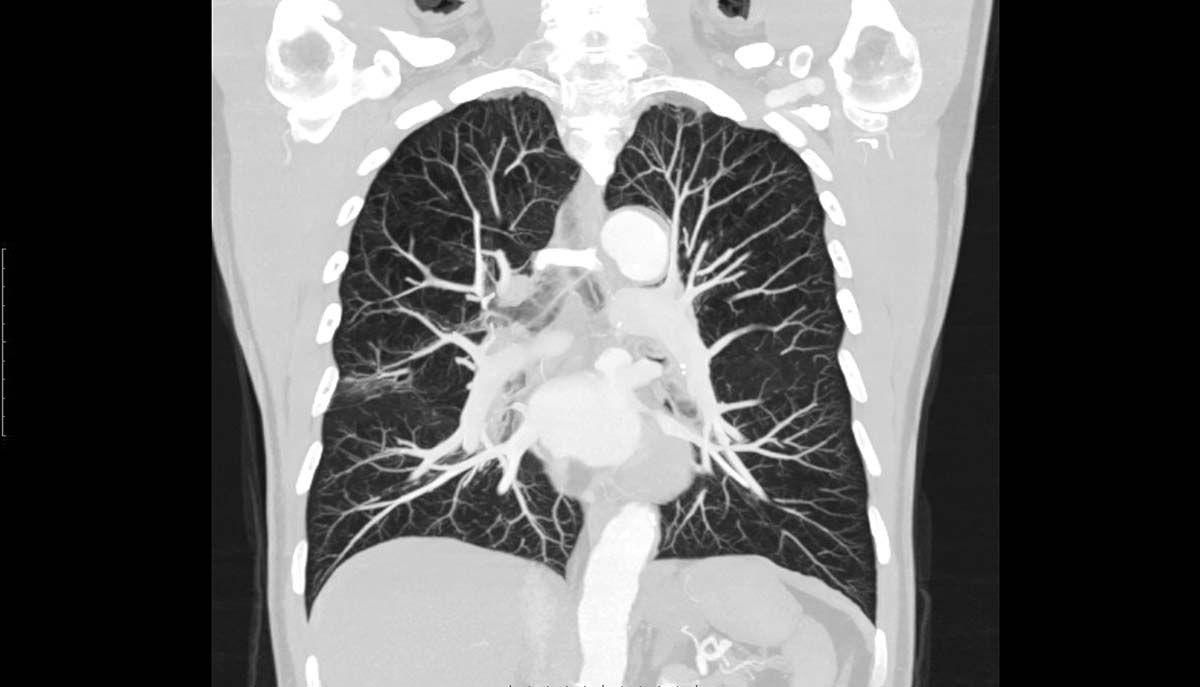
Tot mai des întâlnită în lumina progreselor dispozitivelor imagistice, EPDA poate evolua asimptomatic sau simptomele sale pot fi atribuite altei patologii.
Embolia pulmonară (EP) înseamnă un embol, cel mai frecvent un tromb, blocat la nivelul unei ramuri arteriale pulmonare sau chiar la bifurcaţia arterelor pulmonare în cazul trombilor de dimensiuni mai mari.
EP descoperită accidental (EPDA) este o parte integrantă a tromboembolismului venos (TEV), o entitate care include tromboza venoasă profundă (TVP) și EP.
În EDPA, embolii sunt detectaţi pe tomografii computerizate toracice efectuate pentru alte motive decât o suspiciune de EP (1). Societatea Internaţională de Tromboză și Hemostază favorizează termenul de „accidentală”, și nu „asimptomatică”, întrucât deseori pacienţii cu EPDA prezintă simptome atribuite unor alte cauze (2).
Rata anuală a EP este raportată la 39-115 la 100.000 de locuitori, însă puţine studii au abordat problema EPDA, astfel încât prevalenţa acesteia variază între 0,5 și 5,7% în populaţii neselecţionate, mai ridicată în cazul pacienţilor internaţi și cu neoplazii, la aceștia din urmă aproximativ 50% dintre EP fiind descoperite accidental (3,4).
EP face parte dintr-un sindrom cardiovascular care include afectarea coronariană, cerebrală și arterială periferică. Formarea unui tromb pornește de la cei trei factori din triada Virchow: stază, hipercoagulabilitate și leziunea endoteliului vascular, însă inflamaţia joacă și ea un rol important (5,6).
Localizările predilecte ale trombilor venoși sunt la nivelul sistemului venos profund al membrelor inferioare, dar și al pelvisului, membrului superior și cavităţilor cardiace drepte. Factorii favorizanţi ai EP sunt multipli și uneori greu de obiectivat: stări de hipercoagulabilitate, imobilizare, neoplazii, stază venoasă, sarcină, contraceptive orale, estrogeni, intervenţii chirurgicale și condiţii genetice (7).
TEV este de patru-șapte ori mai comun la pacienţii cu neoplazii, aceștia având factori de risc cumulativi suplimentari (intervenţii chirurgicale, spitalizări, chimioterapie, terapie hormonală etc.) (8).
Consecinţele EP sunt respiratorii (creșterea spaţiului mort alveolar, hipoxemie, hiperventilaţie, pierderea surfactantului, mai rar infarct pulmonar) și hemodinamice (creșterea rezistenţei vasculare a patului pulmonar, accentuarea postsarcinii ventriculului drept, eventual insuficienţă cardiacă dreaptă), atât prin obstrucţie, cât și prin mecanisme neuroumorale (1,5,7).
Hipertensiunea pulmonară cronică se poate instala dacă EP sunt recurente sau prin persistenţa embolului iniţial (5,7).
EP este potenţial letală, iar întârzieri în diagnostic pot să apară din cauză că pacienţii cu această afecţiune pot fi asimptomatici sau se pot prezenta cu simptome nespecifice, EP fiind supranumită „the great pretender” (din engleză, „marele prefăcut”).
Semnele și simptomele de EP includ dispnee (cel mai des), durere toracică, tahicardie (cel mai comun semn), hipotensiune, semne clinice de TVP, dar pot fi prezente și sincopa, durerea pleuritică (EP mic, periferic),
moartea subită cardiacă (1,5). În cazul EPDA, prin excelenţă lipsește suspiciunea clinică de EP.
Odată cu creșterea calităţii evaluărilor imagistice, EPDA a devenit tot mai frecventă (4). Nu se recomandă investigarea pentru EP a oricărui pacient cu dispnee sau durere toracică, deși un grad de suspiciune trebuie să existe (1). Atunci când se ridică o suspiciune clinică de EP, ghidurile actuale recomandă un algoritm diferenţiat în funcţie de stabilitatea hemodinamică documentată după evaluarea clinică.
Scorul Geneva de predicţie clinică se va folosi pentru a stabili probabilitatea clinică. Apoi se va evalua imagistic (ecocardiografie, angiografie pulmonară prin tomografie computerizată, tomografie computerizată cu substanţă de contrast intravenos, scintigrafie de ventilaţie/perfuzie, angiografie pulmonară etc.) și prin D-dimeri (kit cu sensibilitate înaltă) (1).
Ghidul Societăţii Europene de Cardiologie sugerează teste imagistice suplimentare atunci când la tomografia computerizată sunt găsite defecte de umplere cu contrast izolate subsegmentare, pentru a se confirma EP(1).
În cazul EDPA, algoritmul diagnostic de EP nu se aplică, întrucât evaluarea imagistică, de obicei tomografie computerizată, este efectuată cu o altă indicaţie decât suspiciunea de EP, iar diagnosticul este stabilit
accidental.
Evaluarea severităţii EP se va face odată ce EPDA a fost diagnosticată, conform indexului PESI (Pulmonary Embolism Severity Index), în forma originală sau simplificată, care estimează riscul de mortalitate, așa cum recomandă Ghidul European, acesta fiind prezentat în tabelele 1 și 2 (1).

În contextul ischemiei ventriculare drepte consecutive, valorile troponinei înalt sensibile pot fi crescute, ca și valorile peptidelor natriuretice. Ecografia venoasă poate fi indicată pentru a găsi eventuale surse de trombi, iar electrocardiograma poate evidenţia patternul S1Q3T3, însă nespecific în lipsa suspiciunii de EP. Pot fi prezente și tahicardia și semnele de supraîncărcare dreaptă, P pulmonar, deviaţia axială dreaptă, blocul de ram drept nou apărut.
Se poate efectua și o evaluare pentru hipercoagulabilitate/trombofilie, incluzând teste pentru antitrombina III, proteinele C și S, anticoagulant lupic, neoplasme oculte, boli de colagen (7).
Deși încărcătura embolică pare mai redusă în cazul EPDA decât la EP simptomatice, studiile observaţionale ilustrează un risc similar de TEV și de mortalitate (9). La pacienţii oncologici, unde studiile recente sunt mai numeroase, evoluţia clinică este paralelă cu cea din EP simptomatică, metaanalizele subliniind necesitatea unei conduite terapeutice în
consecinţă (10).
Însăși abordarea terapeutică a EP simptomatică subsegmentară este grevată de controverse, astfel încât pentru EPDA subsegmentară datele disponibile sunt și mai puţine. Ghidul Societăţii Europene de Cardiologie menţionează că tratamentul EPDA asimptomatice la pacienţii fără cancer reprezintă un important punct în care dovezile sunt insuficiente.
Pentru pacienţii neoplazici, EPDA se va gestiona similar cu EP
simptomatică dacă sunt implicate ramuri segmentare sau mai proximale, ramuri subsegmentare multiple sau doar una singură în combinaţie cu o TVP documentată (1).
Ghidul American (CHEST) și cel al Societăţii Americane de Oncologie Clinică sugerează măsuri similare de anticoagulare ca pentru EP simptomatică, dar dovezile sunt considerate insuficiente, deși notează că studiile observaţionale indică o evoluţie similară pentru EP simptomatică și EPDA (11,12).
Managementul EPDA implică trei etape: confirmarea EP eventual prin angiografie pulmonară prin tomografie computerizată, evaluarea riscului de sângerare și stabilirea strategiei terapeutice (3). De notat că pacienţii neoplazici au uneori un risc de sângerare crescut (trombocitopenie, afectare hepatică în urma tratamentului, fragilitate vasculară, invazia
tumorală a unor vase de sânge).
Citiți și: Ce este nou privitor la tulburările interacţiunii intestin-creier?
Material preluat din volumul „Cardiologie 2022 – Tromboembolismul pulmonar”, editat de „Viaţa Medicală”.
Bibliografie
1. Konstantinides SV, Meyer G, Becattini C, Bueno H, Geersing GJ, Harjola VP, Huisman MV, Humbert M, Jennings CS, Jiménez D, Kucher N, Lang IM, Lankeit M, Lorusso R, Mazzolai L, Meneveau N, Ní Áinle F, Prandoni P, Pruszczyk P, Righini M, Torbicki A, Van Belle E, Zamorano JL; ESC Scientific Document Group. 2019 ESC Guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020 Jan 21;41(4):543-603. doi: 10.1093/eurheartj/ehz405
2. Khorana AA, O'Connell C, Agnelli G, Liebman HA, Lee AY; Subcommittee on Hemostasis and Malignancy of the SSC of the ISTH. Incidental venous thromboembolism in oncology patients. J Thromb Haemost. 2012 Dec;10(12):2602-4. doi: 10.1111/jth.12023
3. Delluc A, Wang TF. How to treat incidental pulmonary embolism in cancer patients? Recent advances. Kardiol Pol. 2021;79(12):1305-1310. doi: 10.33963/KP.a2021.0164
4. Caiano L, Carrier M, Marshall A, Young AM, Ageno W, Delluc A, Wang TF. Outcomes among patients with cancer and incidental or symptomatic venous thromboembolism: A systematic review and meta-analysis. J Thromb Haemost. 2021 Oct;19(10):2468-2479. doi: 10.1111/jth.15435
5. Goldhaber SZ. Pulmonary Embolism. In: Braunwald's Heart Disease: A Textbook of Cardiovascular Medicine, Single Volume, 11th Edition by Zipes DP, Libby P, Bonow RO, Mann DL, Tomaselli GF. Elsevier. 2018; 1681:1698. ISBN: 978-0-323-46299-0
6. Glynn RJ, Danielson E, Fonseca FA, Genest J, Gotto AM Jr, Kastelein JJ, Koenig W, Libby P, Lorenzatti AJ, MacFadyen JG, Nordestgaard BG, Shepherd J, Willerson JT, Ridker PM. A randomized trial of rosuvastatin in the prevention of venous thromboembolism. N Engl J Med. 2009 Apr 30;360(18):1851-61. doi: 10.1056/NEJMoa0900241
7. https://emedicine.medscape.com/article/300901 - accesat online pe 10.03.2022
8. Frere C, Farge D. Clinical practice guidelines for prophylaxis of venous thomboembolism in cancer patients. Thromb Haemost. 2016 Sep 27;116(4):618-25. doi: 10.1160/TH16-04-0302
9. Barritt DW, Jordan SC. Anticoagulant drugs in the treatment of pulmonary embolism. A controlled trial. Lancet. 1960;1: 1309–1312. doi: 10.1016/s0140-6736(60)92299-6
10. Liebman HA, O’Connell C. Incidental venous thromboembolic events in cancer patients: what we know in 2016. Thromb Res. 2016 Apr.;140 Suppl 1:S18-20. doi: 10.1016/S0049-3848(16)30093-7
11. Stevens SM, Woller SC, Baumann Kreuziger L, Bounameaux H, Doerschug K, Geersing GJ, Huisman MV, Kearon C, King CS, Knighton AJ, Lake E, Murin S, Vintch JRE, Wells PS, Moores LK. Executive Summary: Antithrombotic Therapy for VTE Disease: Second Update of the CHEST Guideline and Expert Panel Report. Chest. 2021 Dec;160(6):2247-2259. doi: 10.1016/j.chest.2021.07.056
12. Key NS, Khorana AA, Kuderer NM, Bohlke K, Lee AYY, Arcelus JI, Wong SL, Balaban EP, Flowers CR, Francis CW, Gates LE, Kakkar AK, Levine MN, Liebman HA, Tempero MA, Lyman GH, Falanga A. Venous Thromboembolism Prophylaxis and Treatment in Patients With Cancer: ASCO Clinical Practice Guideline Update. J Clin Oncol. 2020 Feb 10;38(5):496-520. doi: 10.1200/JCO.19.01461
13. van der Hulle T, den Exter PL, Planquette B, Meyer G, Soler S, Monreal M, Jiménez D, Portillo AK, O'Connell C, Liebman HA, Shteinberg M, Adir Y, Tiseo M, Bersanelli M, Abdel-Razeq HN, Mansour AH, Donnelly OG, Radhakrishna G, Ramasamy S, Bozas G, Maraveyas A, Shinagare AB, Hatabu H, Nishino M, Huisman MV, Klok FA. Risk of recurrent venous thromboembolism and major hemorrhage in cancer-associated incidental pulmonary embolism among treated and untreated patients: a pooled analysis of 926 patients. J Thromb Haemost. 2016 Jan;14(1):105-13. doi: 10.1111/jth.13172
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe