În aceste luni ale anului 2020, atenţia medicilor și a cercetătorilor se îndreaptă spre descoperirea metodelor de înaltă eficienţă pentru identificarea și tratamentul infecţiei cu SARS-CoV-2.
Laboratoarele clinice se alătură acum Centrelor pentru Controlul și Prevenirea Bolilor (CDC) și laboratoarelor de sănătate publică locale în testarea noului coronavirus. Identificarea prin testare a persoanelor infectate îi va ajuta pe specialiștii din domeniul medical să decidă care bolnavi ar trebui să fie izolaţi și să primească îngrijiri la timp și îi ajută pe experţii în sănătate publică să urmărească răspândirea virusului.
SARS-CoV-2 este un virus cu un genom ARN înconjurat de un nucleocapsid de simetrie elicoidală. Pătrunderea coronavirusurilor în celulă depinde de legarea proteinelor cu spiculi virali (S) la receptorii celulari și de amorsarea proteinei S de către proteazele celulelor gazdă. S-a demonstrat că virusul SARS-CoV-2 folosește receptorul ACE2 de la nivelul alveolelor pulmonare pentru intrarea în celule și o enzimă, proteinserina TMPRSS2, pentru amorsarea proteinei S. Un inhibitor TMPRSS2 aprobat pentru utilizare clinică ar putea constitui o opţiune de tratament. Unele rezultate au relevat o comunicare importantă între SARS-CoV-2 și SARS-CoV. Aproximativ 80% dintre infecţiile cu COVID-19 sunt ușoare.
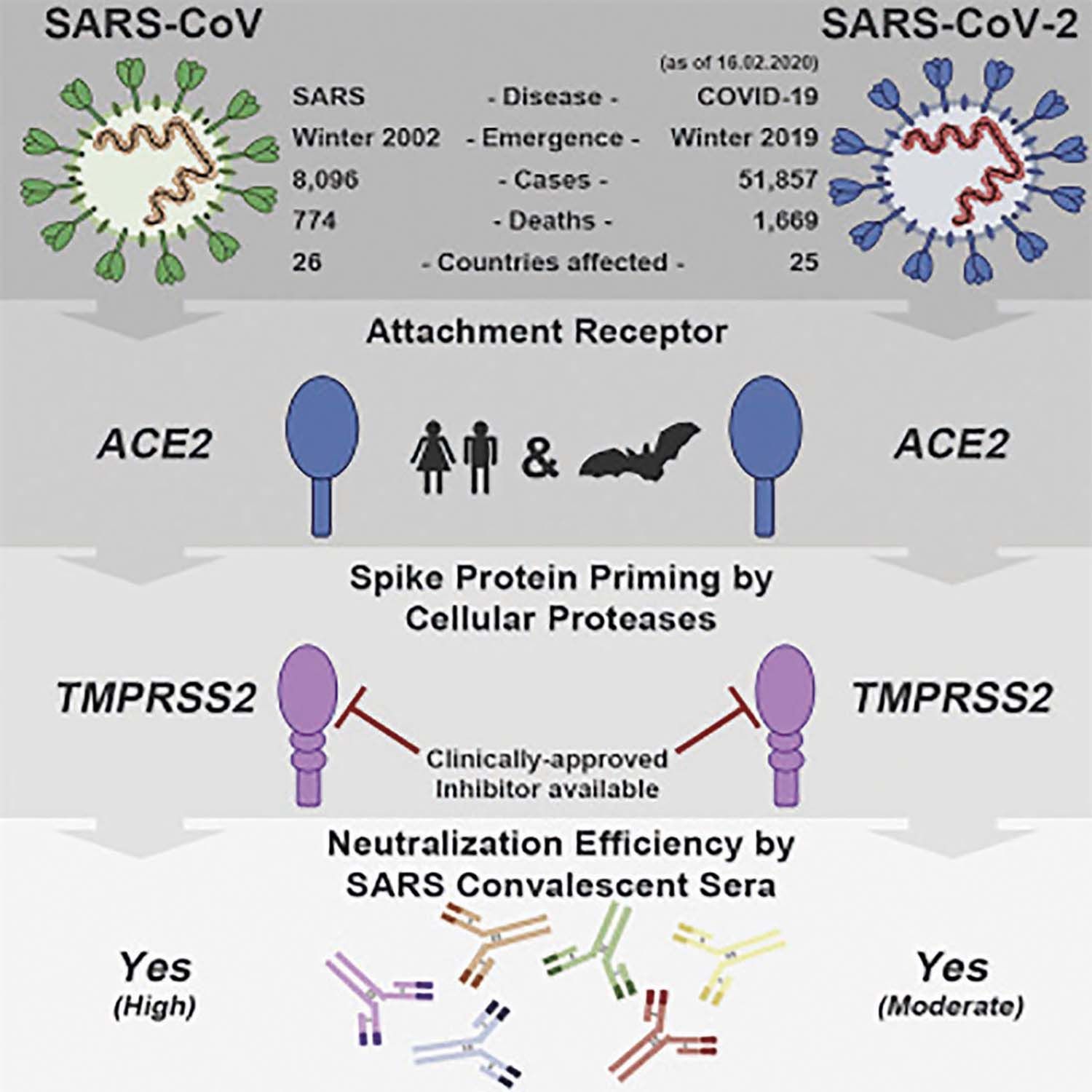
Pacienţii cu SARS-CoV-2 în convalescenţă prezintă un răspuns cu anticorpi neutralizanţi care poate fi detectat chiar și la 24 de luni de la infecţie și care este în mare parte îndreptat împotriva proteinei spike (S), prin care virusul se leagă la receptorii membranari. Vaccinurile SARS experimentale, incluzând proteina S recombinantă și virusul inactivat, induc răspunsurile la anticorpi neutralizanţi. Rezultatele indică faptul că neutralizarea răspunsurilor cu anticorpi împotriva SARS-S ar putea oferi o anumită protecţie împotriva infecţiei cu SARS-CoV-2 (1,2).
1a. Test serologic, cu anticorpi
Există câteva tipuri de teste rapide. Unul este cel serologic, imunologic (o picătură de sânge se recoltează din deget, prin înţepătură) și oferă rezultatele în 20-30 de minute. Testul evidenţiază anticorpii specifici împotriva SARS-CoV-2, respectiv IgM și IgG. Aceste teste nu sunt indicate pentru detectarea infecţiilor active în faza timpurie, deci nu oferă un diagnostic precoce, deoarece devin pozitive la 3-5 zile de la debutul clinic al bolii. Cu alte cuvinte, în cazul unei persoane asimptomatice, care se află la mai mult de 3-5 zile de la debutul bolii, testul poate fi pozitiv. Dacă este negativ pentru o persoană simptomatică, se recomandă repetarea sa la 5 zile, pentru a evidenţia seroconversia, adică trecerea de la absenţa anticorpilor specifici la prezenţa lor.
1b. Test de identificare a antigenului
Al doilea tip de test rapid este cel efectuat din exsudatul nazofaringian, ce are ca scop identificarea antigenului viral. Dă rezultate în 20-30 de minute și este similar cu testele rapide de gripă. Acest test rapid este mai eficient decât testul serologic, deoarece este util și pentru diagnosticul precoce al infecţiei cu SARS-CoV-2. Cercetătorii lucrează la dezvoltarea unui dispozitiv integrat pentru testare care ar putea fi folosit pe teren sau chiar acasă. Testele rapide de identificare directă pentru antigenul SARS-CoV-2 nu există momentan pe piaţa românească.
Nicio metodă rapidă de testare nu este perfectă. Orice test duce la o proporţie de rezultate fals-pozitive (cel testat este sănătos, dar testul îl consideră bolnav) și fals-negativ (cel testat este bolnav, dar testul îl consideră sănătos).
Teste care utilizează abordări cantitative RT-PCR (qRT-PCR) pentru detectarea virusului în 4-6 ore au fost dezvoltate de mai multe laboratoare. Cu toate acestea, timpul necesar pentru depistarea și diagnosticarea pacienţilor suspectaţi de SARS-CoV-2 s-a extins la peste 24 de ore, având în vedere necesitatea de a trimite probe peste noapte la laboratoarele de referinţă. Pentru a impulsiona descoperirile, pe 28 februarie, Administraţia pentru Medicamente și Alimente (FDA) din Statele Unite le-a permis laboratoarelor private acreditate să raporteze rezultatele testelor dezvoltate pe cont propriu, în așteptarea primirii aprobării prin procedură accelerată.
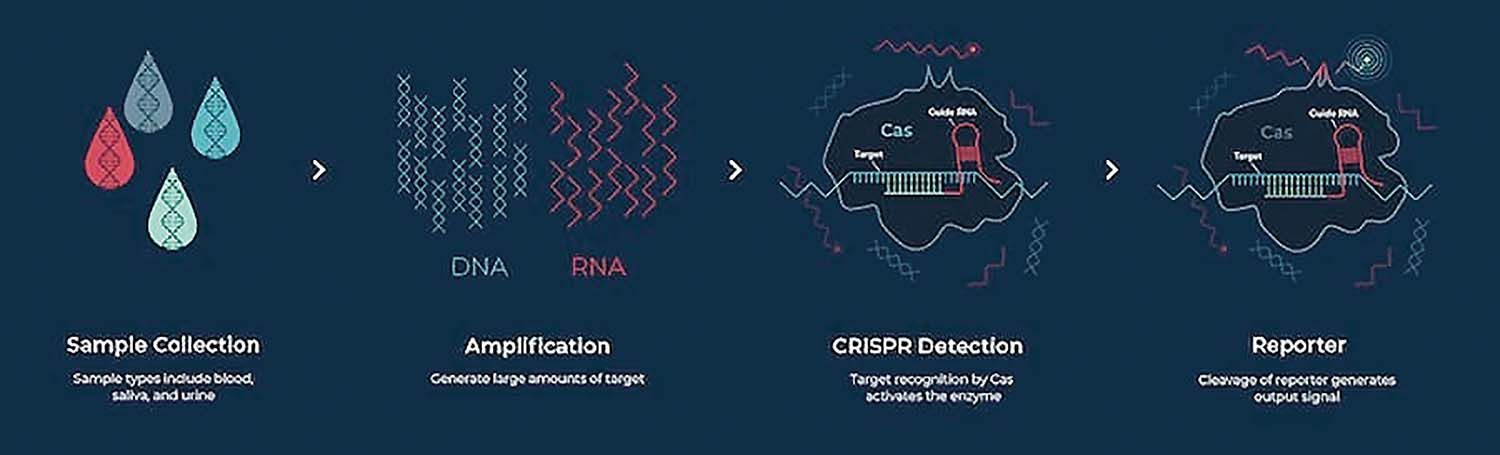
O soluţie o reprezintă tehnologia CRISPR-Cas12-13, un program simplu și foarte versatil bazat pe un panel genetic care analizează concomitent secvenţierea lanţului ARN și ADN. Testul permite oferirea unui rezultat privind prezenţa sau absenţa SARS-CoV-2 în 30-40 de minute. Spre deosebire de metodele bazate pe RT-PCR, metodele de detectare a acidului nucleic bazate pe CRISPR pot funcţiona la o temperatură constantă (de exemplu, 37°C), fără a fi nevoie de un cicler termic scump.
Metoda are numeroase avantaje, prin capacitatea de a analiza de la una la mii de probe simultan, capacitatea de a verifica fiecare eșantion pentru modificări ale secvenţei multiple în ARN. Nucleazele vizate, Cas12a și Cas13a, le-au oferit cercetătorilor capacitatea de a manipula practic orice secvenţă genomică, permiţând crearea ușoară a liniilor de celule izogene pentru studiul bolii umane și promovând noi posibilităţi interesante pentru terapia genică umană. În timp ce Cas12a este specific ADN-ului, Cas13a funcţionează cu ARN. O caracteristică a nucleazelor Cas12 și Cas13 este faptul că acestea prezintă activitate de clivare trans- sau colaterală.
Spre deosebire de metodele bazate pe PCR, metodele de detectare a acidului nucleic bazate pe CRISPR pot funcţiona la o temperatură constantă (de exemplu, 37°C), fără a fi nevoie de un cicler termic scump.

Există mai multe protocoale de detecţie a virusului SARS-CoV-2 prin tehnologia CRISPR. De exemplu, SHERLOCK DETECTER – Specific High Sensitivity Enzymatic Reporter UnLOCKing. Aceasta implică trei etape:
Noul test SARS-CoV-2 DETECTER este printre primii care folosesc tehnologia de orientare a genelor CRISPR pentru a testa prezenţa noului coronavirus. Întrucât CRISPR poate fi modificat pentru a viza orice secvenţă genetică, producătorii kitului de testare l-au „programat” în două regiuni-ţintă din genomul noului coronavirus. Una dintre aceste secvenţe este comună tuturor coronavirusurilor „asemănătoare cu SARS”, în timp ce cealaltă este unică pentru SARS-CoV-2, care provoacă COVID-19. Testarea prezenţei ambelor secvenţe asigură că noul instrument DETECTER poate face distincţia între SARS-CoV-2 și virusurile strâns legate de acesta.
Noul test este, de asemenea, extrem de sensibil, poate detecta prezenţa a 10 coronavirusuri în 1 microlitru de lichid prelevat de la pacient – un volum de sute de ori mai mic decât o picătură de apă. Deși ușor mai puţin sensibile decât testele tip RT-PCR existente, care pot detecta 3,2 copii ale virusului pe 1 microlitru, diferenţa este puţin probabil să aibă un impact vizibil în diagnosticare, deoarece pacienţii infectaţi au de obicei sarcini virale mult mai mari. SARS-CoV-2 DETECTER se adaugă la o suită de creștere rapidă a noilor teste de diagnostic COVID-19 prin care cercetătorii și clinicienii speră că vor crește capacitatea de testare.
Pe măsură ce specialiștii lucrează la validarea noului test CRISPR DETECTER cu aprobarea FDA, producătorii continuă să facă modificări la kitul de testare, astfel încât să poată fi utilizat pentru testarea pe teren (aeroport, școli), clinici mici.
Nicio metodă de testare nu este perfectă. Orice test duce la o proporţie de rezultate fals-pozitive și fals-negative. Încă nu avem suficiente date pentru a cunoaște procentul acestor tipuri de rezultate în cazul COVID-19. Având în vedere posibilitatea unor rezultate fals-negative, Organizaţia Mondială a Sănătăţii susţine că un rezultat negativ al testului nu elimină posibilitatea infecţiei cu COVID-19 și recomandă testarea multiplă.
Evidenţierea SARS-CoV-2 prin metoda ELISA
Prin enzyme-linked immunosorbent assay (ELISA), anticorpul IgM sau IgG se leagă cu afinitate ridicată atât de SARS-CoV, cât și de SARS-CoV-2 – mai exact, de fragmente din proteina S (spike). Tehnica indică un potenţial pentru dezvoltarea testelor de diagnostic, fie ca teste de captare a virusului, fie ca și controale în teste serologice care măsoară răspunsul imun după expunerea la virus. Izotipurile umane IgG1, IgG3, IgM și IgA sunt disponibile pentru a simula răspunsurile în anticorpi observate în COVID-19.
Testele de laborator, adiţionale în cazul COVID-19, au arătat valori mai mari comparativ cu valorile de referinţă în cazul unor indicatori precum formula leucocitară (neutrofilie cu limfopenie), numărul de trombocite, proteina C-reactivă, fibrinogenul, VSH, interleukina-6, aspartate amino transferaza (AST), timpul de trombină (TT) și D-dimerii, cu predispoziţie la tromboze.
Modulul Smart Gene® NGS se bazează pe un sistem de reţea de baze de date integrat. Metoda de analiză genetică poate fi aleasă de utilizator pentru a detecta o varietate de meniuri microbiene. Anterior, analizorul inteligent a fost utilizat pentru a caracteriza cu exactitate o varietate de bacterii.
Smart Gene intenţionează să introducă în viitor software-ul automat de analiză a secvenţierii virusurilor. Pentru a reduce la minimum proporţia de rezultate negative, se recomandă testarea suplimentară a probelor colectate din aparatul respirator în cazurile foarte suspecte și verificarea calităţii eșantionului prin testarea PCR.
Aceste teste detectează ARN-ul coronavirusului și, prin aceasta, infecţiile active. Testul este fiabil numai în prima săptămână a bolii. Virusul migrează apoi mai departe în plămâni și devine dificil de detectat folosind tampoane nazale sau din gât.
Există mai multe platforme PCR. Proba poate fi prelevată din secreţii respiratorii, exsudat nazofaringian, aspirat bronșic sau lavaj bronhoalveolar, la pacientul intubat orotraheal, la care nu avem niciun diagnostic și la care testul din exsudat a fost negativ. Timpul de așteptare variază, în funcţie de platforma folosită, de la 45 de minute la 6 ore. Dacă vorbim despre tehnici automate, rezultatele sunt obţinute în 45 de minute, iar dacă este nevoie de o pregătire anterioară, trebuie respectate anumite etape care trebuie făcute manual, iar rezultatele se obţin în aproximativ 6 ore.
RT-PCR (reacţie de polimerizare în lanţ în timp real) este o metodă de laborator folosită pentru realizarea unui număr foarte mare de cópii ale secţiunilor scurte de ADN dintr-un eșantion foarte mic de ADN, astfel încât să poată fi detectat. Acest proces se numește „amplificarea” ADN-ului. SARS-CoV-2 fiind un virus ARN, va trebui să fie transformat în ADN înainte de a putea fi amplificat. În timpul testului, enzima revers transcriptază se leagă de ARN-ul cu catenă unică al virusului și realizează o copie ADN care poate fi amplificată prin procesul obișnuit de PCR. Dacă într-o probă este prezentă o cantitate suficientă de ARN viral, acesta va fi amplificat și detectat, iar testul va fi pozitiv.
În cazul în care probele sunt trimise la laboratoare de referinţă pentru a fi procesate, primirea rezultatelor poate dura câteva zile.
Metodele de screening prezentate, bazate pe reacţia antigen-anticorp (Ag-Ac), cu specificitate și sensibilitate de 50-80% în diagnosticarea infecţiei cu SARS-CoV-2, pot fi alese de laboratoarele specializate în funcţie de numărul de pacienţi și necesită teste suplimentare de confirmare.
Deocamdată, testele RT-PCR sunt standardul de aur în diagnosticul COVID-19, singurele validate de Organizaţia Mondială a Sănătăţii.
Bibliografie
1. Tian X1, Li C1, Huang A1, Xia S1, Lu S1 et al. Potent binding of 2019 novel coronavirus spike protein by a SARS coronavirus-specific human monoclonal antibody. Emerg Microbes Infect. 2020; 9(1): 382-385. doi: 10.1080/22221751.2020
2. Pruett-Miller SM, Reading DW, Porter SN, Porteus MH. 2009. Attenuation of zinc finger nuclease toxicity by small-molecule regulation of protein levels. PLoS Genet 5: e1000376
3. Myhrvold, C. et al. Field-deployable viral diagnostics using CRISPR-Cas13. Science. 2018; 360, 444–448
4. Simmon KE, Croft AC, Petti CA. Application of Smart Gene IDNS Software to Partial 16S rRNA Gene Sequences for a Diverse Group of Bacteria in a Clinical Laboratory. Journal of Clinical Microbiology 2006; 44(12): 4400-4406. doi: 10.1128/JCM.01364-06.
5. Qian Q, Tang YW, Kolbert CP, et al. Direct identification of bacteria from positive blood cultures by amplification and sequencing of the 16s rRNA gene: evaluation of BACTEC 9240 instrument true-positive and false-positive results. J Clin Microbiol. 2001; 39: 3578-3582
6. Amanat F, Nguyen T, Chromikova V, Strohmeier S, Stadlbauer D, et al. View ORCID Profile Jussi Hepojoki, Viviana Simon, Florian Krammer A serological assay to detect SARS-CoV-2 seroconversion in humans. MedRxiv 2020. https://doi.org/10.1101/2020.03.17.20037713
7. Laboratories Working to Expand COVID-19 Testing. www.aacc.org | www.labtestsonline.org
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe