Structura şi funcţiile rezistinei
Rezistina
(denumită şi FIZZ3 – found in
inflammatory zones, identificată în zonele inflamatorii – sau ADSF – adipocyte secreted factor, factor
secretat de adipocite) a fost descoperită ca adipokină în 2001, pornind de la
ipoteza că ţesutul adipos secretă un hormon care mediază insulinorezistenţa şi
că tiazolidindionele inhibă chiar secreţia acestui hormon. Rezistina este o
proteină de 12,5 kDa aparţinând unei familii de proteine denumite molecule rezistin-like (RELM – resistin-like molecule), caracterizată
printr-un conţinut bogat de reziduuri de cisteină la capătul C-terminal; este
un polipeptid cu 94 de aminoacizi, 11 din ei fiind reprezentaţi de cisteină. 10
din cele 11 molecule de cisteină se găsesc la nivelul capătului C-terminal, la
distanţe egale între ele pentru toţi membrii familiei RELM, constituindu-se în
regiunea înalt conservată a familiei de proteine rezistin-like şi contribuind la realizarea de punţi disulfidice
intramonomerice; cea de-a unsprezecelea, situată în poziţia 26, este implicată
în realizarea punţilor disulfurice dintre trimerii de rezistină.
Fiecare
monomer de rezistină cuprinde: un capăt C-terminal cu punţi disulfurice intramonomerice
(Cys35-Cys88, Cys47-Cys87, Cys56-Cys73, Cys58-Cys75 şi Cys62-Cys77), ceea ce îi
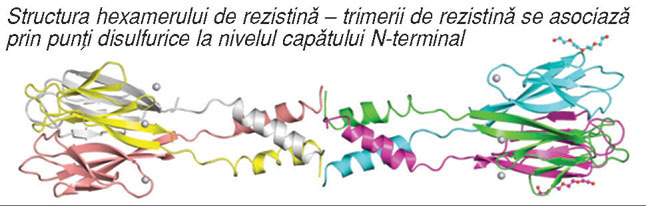
dă aspectul de „sandwich“/globular; un capăt N-terminal cu structură α-helicoidală(v. fig.)
La nivelul
capetelor N-terminale cu structură de α-helix se realizează punţi disulfurice
intermonomerice (prin resturile de cisteină din poziţia 26), care contribuie la
formarea de structuri trimerice, respectiv hexamerice, forma circulantă
predominantă a rezistinei.
La şoareci,
rezistina este sintetizată îndeosebi la nivelul ţesutului adipos alb, în timp
ce la om nivelurile de ARNm pentru rezistină din ţesutul adipos alb sunt foarte
scăzute, uneori nedetectabile. În schimb, s-au decelat niveluri crescute de
ARNm pentru rezistină în măduva osoasă, plămâni, celulele stromale ale ţesutului
adipos, placentă, celulele pancreatice insulare, celulele sistemului
monocito-macrofagic.
Gena care
controlează la om sinteza de rezistină (RETN) este situată la nivelul
cromozomului 19. Expresia genei rezistinei este inhibată de tiazolidindione,
care acţionează in vitro prin
supraexpresia receptorului PPARγ; studiile in
vivo au fost însă discordante, descriindu-se atât up-reglarea, cât şi down-reglarea
genei rezistinei sub acţiunea tiazolidindionelor, ceea ce demonstrează că
efectele antidiabetice ale acestora nu sunt datorate exclusiv interacţiunii lor
cu rezistina. Expresia genei rezistinei a fost de asemenea stimulată in vitro prin administrarea de
endotoxine sau de citokine proinflamatorii pe culturi de monocite umane.
Administrarea de TNFα pe culturile de adipocite umane a
determinat însă scăderea producţiei de rezistină atât la nivel proteic, cât şi
genetic. IL-6 a crescut expresia genei rezistinei pe culturile de monocite din
sângele periferic uman, dar nu a mai avut acelaşi efect şi pe culturile de
adipocite umane. Rezultatele contradictorii ale acestor studii s-ar putea
datora diferitelor linii celulare sau metodologiei utilizate.
Efectele
insulinei asupra sintezei de rezistină sunt de asemenea echivoce: studiile pe
culturile de adipocite au arătat atât scăderea expresiei genei rezistinei (prin
mecanisme independente de calea fosfatidil-inozitol 3-kinazei sau a p38 MAPK),
cât şi creşterea expresiei genei rezistinei atât după stimularea acută, cât şi
cea cronică a adipocitelor cu insulină. Hiperglicemia determină creşterea
sintezei de rezistină atât in vitro,
pe culturi de adipocite, cât şi in vivo.
Dexametazona
creşte sinteza de rezistină atât in vitro,
pe celulele adipocitare, cât şi in vivo,
la nivelul ţesutului adipos alb al şobolanilor. Hormonul de creştere pare să
fie de asemenea un stimulent al secreţiei de rezistină – tratamentul acut sau
continuu cu somatropinum a determinat creşterea expresiei genei rezistinei la
nivelul ţesutului adipos alb. Homocisteina, un binecunoscut factor de risc
cardiovascular, este un alt factor umoral care induce expresia şi secreţia
rezistinei pe adipocitele de şoarece.
Receptorul specific
pentru rezistină nu a fost încă descoperit – un studiu recent pe celulele
stromale progenitoare ale ţesutului adipos a demonstrat legarea rezistinei de
un produs obţinut din clivarea decorinei (îndepărtarea lanţului de
glicozaminoglican al acestuia), care a fost propus ca receptor prin care
rezistina ar promova diferenţierea şi expansiunea ţesutului adipos. Alţi receptori
propuşi a media efectele rezistinei sunt: toll-like
receptor 4 (TLR4), un receptor de pe suprafaţa celulelor inflamatorii de care
se leagă lipopolizaharidele de la suprafaţa celulelor bacteriene (rezistina
competiţionează cu acestea şi se pare că în acest fel îşi exercită o parte din
efectele proinflamatorii) şi respectiv receptorul orfan de tip tirozinkinazic
de la şoarece (ROR1); acţionând asupra acestui receptor exprimat la suprafaţa
celulelor preadipocitare 3T3-L1, rezistina promovează adipogeneza şi scăderea
preluării intracelulare a glucozei.
Variaţiile
fiziologice ale secreţiei de rezistină
Nivelurile
serice de rezistină la om sunt mai mari la sexul feminin decât la cel masculin,
în populaţia adultă. În populaţia pediatrică se pare că nivelurile serice de
rezistină cresc odată cu vârsta şi că sunt de asemenea mai mari la sexul
feminin decât la cel masculin.
Rezistina,
capitalul adipos şi profilul lipidic
Gena rezistinei este
înalt exprimată în ţesutul adipos al şoarecilor, rezistina promovând
transformarea celulelor preadipocitare în adipocite mature. Studiile pe oameni
sunt însă contradictorii – o serie de autori au descris secreţia de rezistină
la nivelul ţesutului adipos, în timp ce alţii nu au reuşit să identifice/au
identificat niveluri foarte scăzute ale ARNm pentru rezistină în ţesutul adipos
alb. Rezistina provine în ţesutul adipos uman de la nivelul preadipocitelor şi
al monocitelor din stroma vasculară.
O serie de
studii clinice transversale (tabelul 1) au
arătat că nivelurile serice plasmatice de rezistină sunt corelate pozitiv cu
indicele de masă corporală, fiind crescute mai ales în obezitatea tronculară,
în timp ce alte studii nu au identificat aceste corelaţii.
Corelaţia
rezistinei cu adipozitatea este incertă în populaţia pediatrică (tabelul 2) – există studii care arată o
corelaţie slabă a rezistinei cu adipozitatea tronculară, şi altele care nu
identifică această corelaţie.
În studii
longitudinale, nivelurile serice de rezistină nu s-au modificat în urma scăderii
ponderale la un an; eficienţa efortului fizic sistematizat în ameliorarea
profilului rezistinei este de asemenea incert – există studii care demonstrează
efectele benefice ale activităţii fizice asupra rezistinei copiilor
supraponderali, după cum alte studii au arătat că efortul fizic este ineficient
în absenţa scăderii ponderale.
Studiile in vitro şi in vivo, deşi reduse ca număr, par să sugereze un efect
hiperlipemiant al rezistinei: incubarea cronică a culturilor de miocite cu
rezistină s-a asociat cu scăderea preluării de acizi graşi liberi, printr-un
sistem de semnalizare care a cuprins CD36, proteina de transport a acizilor graşi,
acetil-CoA carboxilaza, proteinkinaza AMP-activată; pe modele animale,
hiperrezistinemia se asociază cu creşterea nivelurilor plasmatice de
trigliceride şi de colesterol total; administrarea de rezistină pe culturile de
hepatocite umane a condus nu doar la scăderea expresiei receptorilor membranari
pentru LDL-colesterol, ci şi la scăderea preluării intracelulare a
LDL-colesterolului stimulate de statine, ceea ce evidenţiază un posibil
mecanism de rezistenţă la acţiunea statinelor remarcată în anumite populaţii.
Rezistina,
rezistenţa la insulină şi riscul metabolic
O serie de
studii in vitro şi in vivo sugerează existenţa unei legături
strânse între hiperrezistinemie şi rezistenţa la insulină.
Studiile in vitroau arătat că administrarea rezistinei determină scăderea preluării
glucozei induse de insulină în culturile de miocite la şoareci, mecanismul
propus fiind cel al inhibării translocării intracelulare a transportorului
GLUT4.
Studiile pe
animale au arătat că:
• La şoareci,
rezistina antagonizează efectele insulinei, determinând intoleranţă la glucoză;
infuzia de rezistină recombinată la animale slabe a determinat apariţia
insulinorezistenţei, în timp ce neutralizarea prin anticorpi a rezistinei pe
modele animale obeze a condus la îmbunătăţirea sensibilităţii la insulină;
• Animalele
cu deficit genetic de rezistină sunt protejate de obezitate, iar nivelurile
serice crescute se asociază cu rezistenţa la insulină. Şoarecii ob/ob knock-out şi pentru rezistină
devin şi mai obezi din cauza scăderii suplimentare a ratei metabolismului, dar
sensibilitatea la insulină este îmbunătăţită, în mare măsură prin creşterea
utilizării glucozei la nivelul ţesutului muscular striat şi al ţesutului
adipos;
• Administrarea
de rezistină recombinată la animale de laborator a determinat intoleranţă la
glucoză şi scăderea acţiunii insulinei;
•
Şoarecii knock-out pentru rezistină
au niveluri mai reduse ale glicemiei à jeun şi o sensibilitate mai mare la acţiunea
insulinei asociate cu o scădere a producerii hepatice de glucoză. În plus, ei şi-au
recuperat complet insulinosensibilitatea hepatică după o prealabilă inducere
prin dietă a insulinorezistenţei. Lipsa rezistinei poate conduce la activarea
AMPK şi consecutiv la scăderea expresiei genelor care conduc la gluconeogeneza
hepatică, un efect hepatic opus adiponectinei;
•
Hiperrezistinemia se asociază la şoarecii transgenici cu creşterea adipozităţii
şi a dimensiunilor adipocitelor şi cu scăderea diferenţierii adipocitelor, dar şi
cu intoleranţă la glucoză, hiperinsulinemie, hipertrigliceridemie, rezistenţă
la insulină la nivelul musculaturii scheletice, ficatului şi ţesutului adipos;
•
Alte studii contradictorii au arătat scăderea expresiei ARNm pentru rezistină
în ţesutul adipos al mai multor modele de rozătoare cu insulinorezistenţă.
Per
ansamblu, hiperrezistinemia determină aşadar rezistenţă la insulină şi
intoleranţă la glucoză prin creşterea producţiei hepatice de glucoză şi
respectiv prin scăderea preluării glucozei la nivelul musculaturii striate.
Studiile la
om au arătat că:
•
Polimorfismul genei rezistinei a fost legat de apariţia obezităţii şi
diabetului;
•
O serie de studii transversale efectuate pe loturi variabile (subiecţi obezi,
subiecţi diabetici) au arătat că nivelurile plasmatice de rezistină sunt
pozitiv şi semnificativ corelate cu insulinorezistenţa (IR). Alte studii au
infirmat însă aceste constatări – nivelurile serice de rezistină nu se corelează
cu IR în populaţia indienilor pima şi nici pe loturi de adulţi sănătoşi
normoponderali;
•
Un studiu populaţional prospectiv a „împăcat“ constatările anterioare –
nivelurile serice de rezistină au fost semnificativ mai mari la persoanele care
au dezvoltat DZ tip 2 după o perioadă de urmărire de 8–10 ani, dar asocierea a
fost atenuată după ajustarea pentru IMC şi pentru secreţia de proteină C
reactivă.
 Controversele
pot fi urmarea designului diferit al studiilor, coexistenţei unor alţi factori
ce pot influenţa insulinosensibilitatea sau chiar efectului paracrin al
rezistinei, ceea ce ar explica slaba corelaţie cu nivelurile sale sistemice.
Controversele
pot fi urmarea designului diferit al studiilor, coexistenţei unor alţi factori
ce pot influenţa insulinosensibilitatea sau chiar efectului paracrin al
rezistinei, ceea ce ar explica slaba corelaţie cu nivelurile sale sistemice.Contradicţiile
dintre rezultatele studiilor menţionate privind relaţia rezistinei cu
obezitatea, IR şi riscul de DZ tip 2 pot să-şi mai găsească o explicaţie în
studiile genetice ale ultimilor ani – polimorfismele care implică un singur
nucleotid ale genei rezistinei (RETN) (SNP – polymorphisms): alela G în
regiunea rs1862513 de la capătul 5’ a fost asociată cu: niveluri crescute de
rezistină, obezitate, rezistenţă la insulină, DZ tip 2; alelele rs1477341,
rs4804765, rs1423096 şi rs10401670 din regiunea 3’ UTR s-au asociat cu niveluri
serice de rezistină în populaţia europeană, în timp ce rs34861192 din regiunea
promoterului şi rs3745368 din regiunea 3’ UTR s-au asociat cu nivelurile serice
de rezistină în populaţia japoneză.
Rezistina
şi riscul cardiovascular
Rezistina şi inflamaţia. În afara
rolului său de promovare a insulinorezistenţei, rezistina este implicată şi în procesele
inflamatorii. Deoarece expresia ARNm pentru rezistină la nivelul celulelor
adipoase este redusă – secreţia de rezistină în „organul endocrin adipos“ fiind
cel mai probabil datorată componentei celulare a stromei vasculare, devine
evident faptul că secreţia de rezistină în obezitate este un marker al inflamaţiei
acestui ţesut.
Studiile pe
culturi celulare au arătat în mod sistematic că citokinele proinflamatorii (TNFα
şi IL-6) au crescut expresia genei rezistinei la nivelul monocitelor din
sângele periferic uman, dar nu şi pe culturi de adipocite. Relaţia este însă
bidirecţională – rezistina la rândul său a crescut expresia IL-6 şi TNFα la
nivelul monocitelor din sângele periferic uman.
În plus,
nivelurile serice de rezistină sunt crescute într-o serie de stări inflamatorii
sistemice: s-au demonstrat corelaţii semnificative între nivelurile plasmatice
de rezistină şi markerii inflamatorii la persoanele cu inflamaţii severe,
concentraţii crescute de rezistină în lichidul sinovial al pacienţilor cu artrită,
niveluri serice crescute în poliartrita reumatoidă sau în boli inflamatorii
intestinale. Mai mult decât atât, s-a descris o corelaţie pozitivă între
nivelurile plasmatice de rezistină şi markerii inflamatori la persoane adulte
asimptomatice, dar la risc pentru ateroscleroză.
Rezistina şi ateroscleroza. Implicarea
rezistinei în aterogeneză este presupusă şi demonstrată atât de studiile
experimentale in vivo şi in vitro, cât şi de rezultatele
studiilor clinice.
Rezistina
are efecte cardiovasculare nefavorabile prin mecanisme multiple: determină
activarea celulelor endoteliale prin stimularea eliberării de endotelină-1; creşte
generarea speciilor reactive de oxigen, cu scăderea consecutivă a sintezei
oxidului nitric la nivelul celulelor endoteliale, efectul cumulat fiind disfuncţia
endotelială; determină creşterea expresiei moleculei de adeziune a celulelor
vasculare VCAM-1 şi a proteinei chemotactice pentru monocite (MCP-1); induce
proliferarea celulelor musculare netede; determină migrarea celulelor musculare
netede pe culturile celulare din peretele aortic la şobolani; pare să stimuleze
transformarea macrofagelor în celule spumoase prin impregnare lipidică;
determină hipertrofie cardiacă prin calea IRS1 (insulin receptor substrate 1)/MAPK (proteinkinaza activată de
mitogeni).
endoteliale, efectul cumulat fiind disfuncţia
endotelială; determină creşterea expresiei moleculei de adeziune a celulelor
vasculare VCAM-1 şi a proteinei chemotactice pentru monocite (MCP-1); induce
proliferarea celulelor musculare netede; determină migrarea celulelor musculare
netede pe culturile celulare din peretele aortic la şobolani; pare să stimuleze
transformarea macrofagelor în celule spumoase prin impregnare lipidică;
determină hipertrofie cardiacă prin calea IRS1 (insulin receptor substrate 1)/MAPK (proteinkinaza activată de
mitogeni).
S-a
identificat prezenţa rezistinei la nivelul leziunilor aterosclerotice atât la şoarece,
cât şi la om, iar studiile populaţionale au arătat că nivelurile plasmatice de
rezistină s-au corelat cu calcificările la nivelul arterelor coronare,
dovedindu-se atât efectul său endocrin, cât şi prin cel paracrin.
Rezistina
pare a se asocia şi cu un risc mai mare de boală cardiovasculară clinic
manifestă: pe un studiu prospectiv, nivelurile serice de rezistină superioare
percentilei 75 s-au asociat cu un risc crescut de infarct miocardic acut şi
niveluri crescute de rezistină au fost descrise şi în serul pacienţilor aflaţi
în faza acută a infarctului miocardic cu supradenivelare de ST, fiind unul din
markerii propuşi pentru această fază a evenimentului coronarian; în studii
prospective, nivelurile serice crescute de rezistină au fost corelate atât cu
un risc mai mare de AVC ischemic, cât şi cu evoluţia nefavorabilă a
cardiomiopatiei dilatative nonischemice.
Rolurile
rezistinei în complicaţiile metabolice şi cardiovasculare ale excesului
ponderal sunt în concluzie incomplet cunoscute şi controversate.
 Controversele
pot fi urmarea designului diferit al studiilor, coexistenţei unor alţi factori
ce pot influenţa insulinosensibilitatea sau chiar efectului paracrin al
rezistinei, ceea ce ar explica slaba corelaţie cu nivelurile sale sistemice.
Controversele
pot fi urmarea designului diferit al studiilor, coexistenţei unor alţi factori
ce pot influenţa insulinosensibilitatea sau chiar efectului paracrin al
rezistinei, ceea ce ar explica slaba corelaţie cu nivelurile sale sistemice. endoteliale, efectul cumulat fiind disfuncţia
endotelială; determină creşterea expresiei moleculei de adeziune a celulelor
vasculare VCAM-1 şi a proteinei chemotactice pentru monocite (MCP-1); induce
proliferarea celulelor musculare netede; determină migrarea celulelor musculare
netede pe culturile celulare din peretele aortic la şobolani; pare să stimuleze
transformarea macrofagelor în celule spumoase prin impregnare lipidică;
determină hipertrofie cardiacă prin calea IRS1 (insulin receptor substrate 1)/MAPK (proteinkinaza activată de
mitogeni).
endoteliale, efectul cumulat fiind disfuncţia
endotelială; determină creşterea expresiei moleculei de adeziune a celulelor
vasculare VCAM-1 şi a proteinei chemotactice pentru monocite (MCP-1); induce
proliferarea celulelor musculare netede; determină migrarea celulelor musculare
netede pe culturile celulare din peretele aortic la şobolani; pare să stimuleze
transformarea macrofagelor în celule spumoase prin impregnare lipidică;
determină hipertrofie cardiacă prin calea IRS1 (insulin receptor substrate 1)/MAPK (proteinkinaza activată de
mitogeni).