Tuberculoza la nivelul sistemului nervos central poate complica evoluţia pacienţilor trataţi cu agenţi anti-TNF, motiv pentru care este absolut obligatorie evaluarea periodică a acestora.
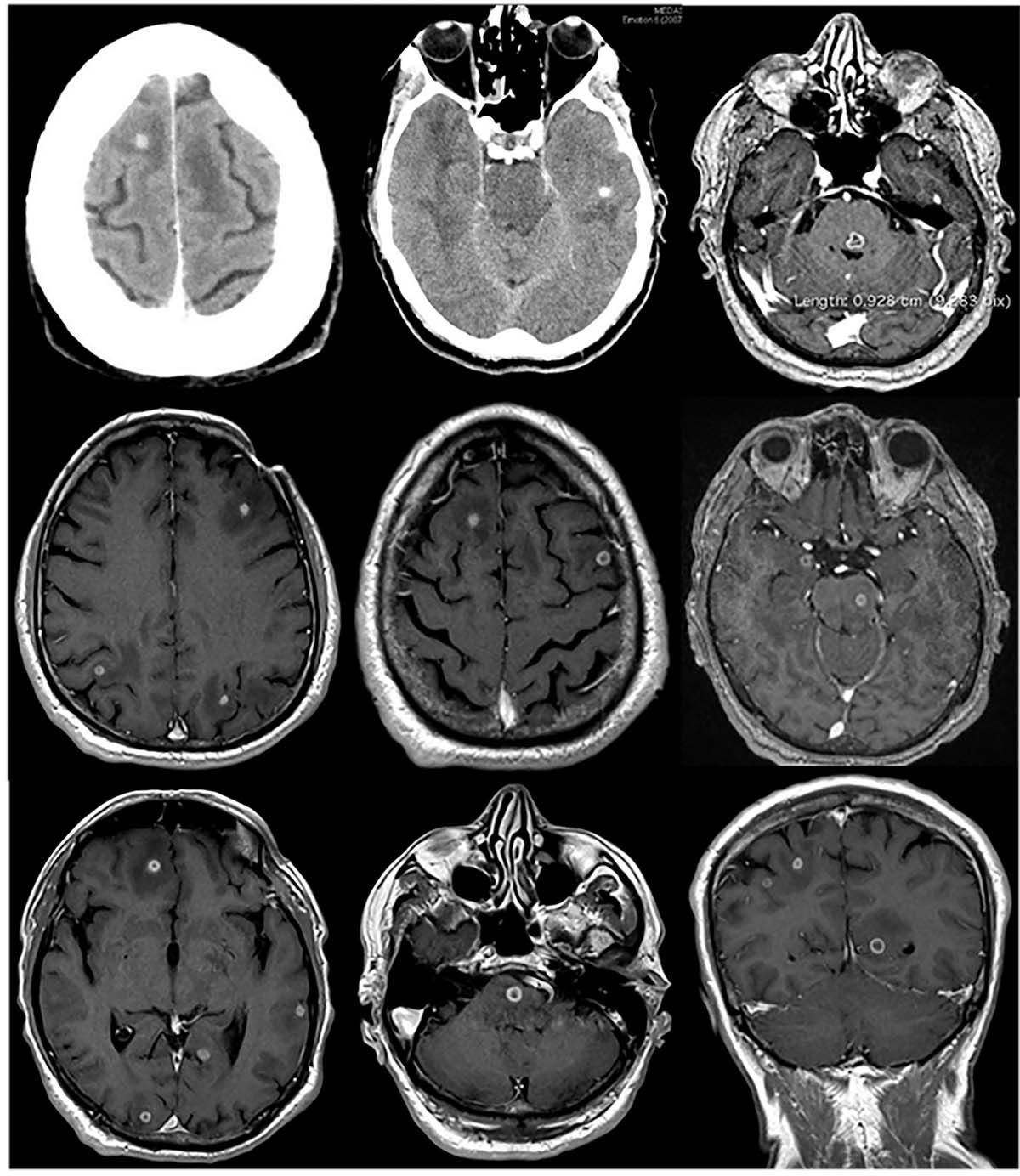
Bărbat de 54 de ani, diagnosticat cu spondilită anchilozantă (SA), tratată cu un agent anti-TNFa (Infliximab), care dezvoltă tuberculoză (TB) cerebrală. IRM (imagistică prin rezonanţă magnetică) cerebral efectuat pentru vertij nesistematizat și diplopie identifică multiple formaţiuni tumorale iodofile cu diametru centimetric situate difuz în toată masa cerebrală însoţite de edem perilezional, mai important la nivelul trunchiului.
La momentul diagnosticului de TB cerebrală nu s-au evidenţiat leziuni pulmonare sugestive pentru TB. Pacientul a primit tratament tuberculostatic, iar evoluţia ulterioară a fost favorabilă. Formele de TB cerebrală sunt extrem de rare, însă formele extrapulmonare trebuie luate în considerare, în contextul în care este cunoscut riscul crescut de a dezvolta TB activă și frecvenţa mai mare de a dezvolta forme extrapulmonare de TB la pacienţii imunosupresaţi.
Spondilita anchilozantă (SA) face parte din grupul spondilartritelor (SpA), un grup de boli inflamatorii interconectate, care prezintă manifestări clinice similare și markeri genetici comuni (1). În timp ce întregul grup al SpA are o prevalenţă de 0,5-1,9%, SA, cel mai mare subgrup, are o prevalenţă de 9 până la 30 de cazuri la 10.000 de locuitori (1,2). În ultimul deceniu, utilizarea agenţilor anti-TNF a constituit un progres important în tratamentul SA. Datorită rolului central al TNFa în mecanismele de apărare, agenţii anti-TNF pot crește susceptibilitatea pacienţilor la diferite tipuri de infecţii, dar mai ales la infecţiile care impun formarea de granuloame (3).
Tuberculoza (TB) continuă să reprezinte o problemă importantă de sănătate publică în ţările subdezvoltate, iar utilizarea agenţilor anti-TNF pentru tratamentul bolilor reumatologice inflamatorii a readus în atenţie această problemă și în ţările cu o incidenţă scăzută a TB, din cauza riscului de reactivare la pacienţii cu infecţie TB latentă (ITBL) (4). Studiile au arătat că toţi agenţii anti-TNF disponibili cresc riscul de a dezvolta TB activă (3).
Pacientul a fost diagnosticat cu SA în 2008, pe baza criteriilor New York modificate (6). Ca urmare a evoluţiei nefavorabile a SA sub tratament cu antiinflamatoare nesteroidiene (AINS) și persistenţei activităţii înalte de boală, luând în considerare recomandările ASAS/EULAR pentru tratamentul SA (9), în mai 2010 este iniţiată terapia cu infliximab 5 mg/kgc la 8 săptămâni.
Conform recomandărilor din protocolul terapeutic în SA din România (5), la iniţierea terapiei biologice s-a efectuat screening pentru ITBL, iar IDR la PPD a fost pozitiv, motiv pentru care s-a administrat chimioprofilaxie cu izoniazidă 300 mg/zi, timp de 9 luni.
În decembrie 2013, pacientul se internează în clinică în regim de urgenţă, prezentând alterarea stării generale, fatigabilitate, febră (38,70 C), transpiraţii profuze, vertij nesistematizat și diplopie, cu ușor sindrom inflamator, fără modificări pleuro-pulmonare și cu multiple formaţiuni tumorale iodofile cu diametru centimetric situate difuz în toată masa cerebrală, însoţite de edem perilezional (Fig. 1).

Pe parcursul internării, pacientul prezintă agravarea simptomatologiei neurologice, asociază bradilalie și strabism. În contextul sindromului febril, corelat cu prezenţa formaţiunilor cerebrale multiple, se decide întreruperea tratamentului cu infliximab și se solicită evaluarea în clinica de Boli infecţioase, unde cazul a fost interpretat drept Toxocara cerebrală (PCR pentru Toxocara pozitiv în LCR). S-a iniţiat terapie antiparazitară cu albendazol și corticosteroizi, terapie sub care evoluţia iniţială a fost favorabilă.
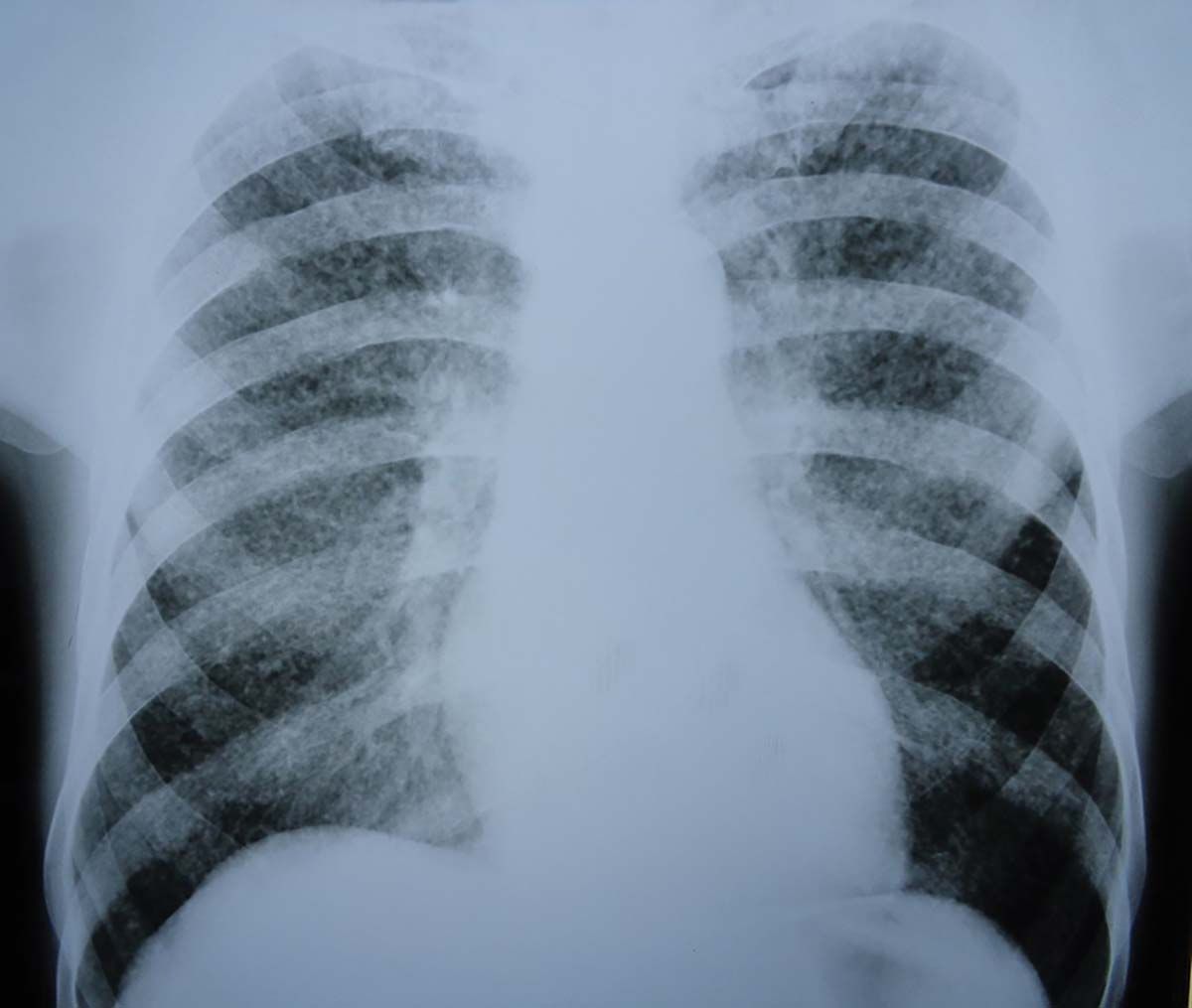
În februarie 2014, la o lună după iniţierea terapiei pentru Toxocara, pacientul se prezintă pentru sindrom febril, iar radiografia toracică efectuată cu această ocazie identifică o imagine radiologică pulmonară rediculo-nodulară sugestivă pentru TB miliară (Fig. 2). Diagnosticul de TB miliară a fost confirmat ulterior prin PCR pozitiv la BK în spută. S-a iniţiat terapia tuberculostatică.
În martie 2014, reapare diplopia, și un nou RMN arată extensia edemului perilezional, dimensiunile leziunilor fiind aparent staţionare. Se decide reluarea terapiei antiparazitare, cu continuarea terapiei tuberculostatice. Din cauza evoluţiei ondulante s-a pus în discuţie etiologia parazitară a leziunilor, intrând în discuţie și posibile tuberculoame cerebrale.
În aprilie 2014, în timp ce era sub tratament tuberculostatic, pacientul se internează în regim de urgenţă într-un serviciu de neurologie/neurochirurgie, prezentând crize convulsive generalizate și diplopie. În urma mai multor investigaţii, inclusiv biopsie cerebrală, se stabilește diagnosticul de meningoencefalită TBC și se modifică schema tuberculostatică, iar evoluţia neurologică este favorabilă.
În septembrie 2014, pacientul prezintă o reactivare clinică și biologică importantă a SA, în contextul renunţării la corticoterapie. Se reia tratamentul cu medrol 4 mg/zi și se adăugă sulfasalazină 2 g/zi, dar nu se reia terapia biologică.
În februarie 2017, examinarea IRM cerebrală nu identifică leziuni endocraniene noi.
În iulie 2019, evoluţia pacientului este favorabilă, motiv pentru care nu se consideră necesară reluarea terapiei biologice.
Cazul ridică mai multe teme de discuţie în ceea ce privește colaborarea interdisciplinară la această categorie de pacienţi.
TB sub anti-TNF
Riscul de a dezvolta TB sub tratament cu agenţi anti-TNF este bine cunoscut. TNFa joacă un rol central în mecanismele de apărare împotriva infecţiei cu M. Tuberculosis prin favorizarea formării și menţinerii granulomului și limitarea acestui tip de infecţie (11). Câteva studii au arătat un risc de TB de până la 30 de ori mai mare la pacienţii trataţi cu anti-TNF faţă de populaţia generală (12,13), iar riscul este mai mare în cazul utilizării anticorpilor monoclonali anti-TNF (ex. infliximab, adalimumab), decât în cazul blocanţilor receptorului solubil al TNF (etanercept) (14,15).
În cazul prezentat, perioada lungă de la iniţierea terapiei anti-TNF (trei ani) până la apariţia simptomelor sugerează mai degrabă o infecţie TB nouă, decât o reactivare a unei ITBL. După o evoluţie iniţială favorabilă, agravarea simptomelor și deteriorarea stării clinice sub terapie tuberculostatică corect condusă sunt descrise ca „reacţie paradoxală”, consecinţa unei activări a răspunsului imun celular împotriva unor antigene somatice eliberate de mycobacteriile distruse. Această reacţie poartă numele de sindrom inflamator de reconstrucţie imună (immune reconstitution inflammatory syndrome, IRIS) (3,17).
TB la nivelul sistemului nervos central reprezintă aproximativ 1% dintre cazurile de TB la nivel mondial și sunt reprezentate de meningita TB sau, mult mai rar, de encefalita TB, tuberculoame sau abcese cerebrale tuberculoase.
Reluarea terapiei anti-TNF după TB
Pacienţii care dezvoltă TB sub tratament cu agenţi anti-TNF de obicei întrerup această terapie cât mai repede posibil, iar decizia de reluare a terapiei, atunci când SA prezintă semne de reactivare a activităţii inflamatorii, este întârziată de riscurile legate de o posibilă reactivare a TB.
Reactivare TB
În ultima perioadă, au fost aprobate mai multe terapii biologice non-anti-TNF pentru tratamentul SA. Datele din studii controlate, registre naţionale de terapii biologice și supravegherea post-marketing arată că riscul de reactivare TB la pacienţii care primesc terapii biologice non-anti-TNF este mai mic și chiar își pun problema dacă screeningul pentru ITBL este cu adevărat necesar.
Mecanismul de acţiune și profilul de siguranţă din studiile clinice indică faptul că secukinumab (SEK) este o variantă sigură în ceea ce privește reactivarea TB și poate reprezenta o opţiune terapeutică bună la pacienţii cu SA cu risc crescut de TB (4,23).
La pacienţii cu TB trebuie făcut un screening atent înainte de iniţierea terapiei cu agenţi anti-TNF, dar și un screening periodic, indiferent de rezultatul testelor la momentul iniţierii terapiei anti-TNF.
TB la nivelul SNC constituie o complicaţie redutabilă, care poate complica evoluţia pacienţilor trataţi cu agenţi anti-TNF. Din cauza posibilei evoluţii fatale, evaluarea periodică atentă a acestor pacienţi este absolut obligatorie.
În cazul pacienţilor cu un risc crescut de a dezvolta sau reactiva TB, agenţii non-anti-TNF ar putea reprezenta o metodă mai sigură de tratament.
Bibliografie
1. Hochberg MC, editor. Rheumatology. Sixth edition. Philadelphia, PA: Mosby/Elsevier; 2015. 2 p.
2. Wang R, Ward MM. Epidemiology of axial spondyloarthritis: an update. Curr Opin Rheumatol 2018;30:137-43.
3. Hess S, Hospach T, Nossal R, Dannecker G, Magdorf K, Uhlemann F. Life-threatening disseminated tuberculosis as a complication of TNF-α blockade in an adolescent. Eur J Pediatr 2011;170:1337-42.
4. Cantini F, Nannini C, Niccoli L, Petrone L, Ippolito G, Goletti D. Risk of Tuberculosis Reactivation in Patients with Rheumatoid Arthritis, Ankylosing Spondylitis, and Psoriatic Arthritis Receiving Non-Anti-TNF-Targeted Biologics. Mediators of Inflammation 2017;2017:1-15.
5. Protocol terapeutic SA - http://www.ms.ro/wp-content/uploads/2018/06/Anexa_Ordin_protocoale_iunie_2018_forma_finala.pdf.
6. Linden SVD, Valkenburg HA, Cats A. Evaluation of Diagnostic Criteria for Ankylosing Spondylitis. Arthritis & Rheumatism 1984;27:361-8.
7. Rudwaleit M, van der Heijde D, Landewé R, Listing J, Akkoc N, Brandt J, et al. The development of Assessment of SpondyloArthritis international Society classification criteria for axial spondyloarthritis (part II): validation and final selection. Ann Rheum Dis 2009;68:777-83.
8. Rudwaleit M, van der Heijde D, Landewé R, Akkoc N, Brandt J, Chou CT, et al. The Assessment of SpondyloArthritis International Society classification criteria for peripheral spondyloarthritis and for spondyloarthritis in general. Ann Rheum Dis 2011;70:25-31.
9. Braun J, van den Berg R, Baraliakos X, Boehm H, Burgos-Vargas R, Collantes-Estevez E, et al. 2010 update of the ASAS/EULAR recommendations for the management of ankylosing spondylitis. Annals of the Rheumatic Diseases 2011;70:896-904.
10. van der Heijde D, Ramiro S, Landewé R, Baraliakos X, Van den Bosch F, Sepriano A, et al. 2016 update of the ASAS-EULAR management recommendations for axial spondyloarthritis. Annals of the Rheumatic Diseases 2017;76:978-91.
11. Wallis RS. Tumour necrosis factor antagonists: structure, function, and tuberculosis risks. Lancet Infect Dis 2008;8:601-11.
12. Brassard P, Kezouh A, Suissa S. Antirheumatic drugs and the risk of tuberculosis. Clin Infect Dis 2006;43:717-22.
13. Wallis RS. Infectious complications of tumor necrosis factor blockade. Curr Opin Infect Dis 2009;22:403-9.
14. Fonseca JE, Canhão H, Silva C, Miguel C, Mediavilla MJ, Teixeira A, et al. [Tuberculosis in rheumatic patients treated with tumour necrosis factor alpha antagonists: the Portuguese experience]. Acta Reumatol Port 2006;31:247-53.
15. Tubach F, Salmon D, Ravaud P, Allanore Y, Goupille P, Bréban M, et al. Risk of tuberculosis is higher with anti-tumor necrosis factor monoclonal antibody therapy than with soluble tumor necrosis factor receptor therapy: The three-year prospective French Research Axed on Tolerance of Biotherapies registry. Arthritis Rheum 2009;60:1884-94.
16. Wallis RS. Mathematical modeling of the cause of tuberculosis during tumor necrosis factor blockade. Arthritis Rheum 2008;58:947-52.
17. Breen R a. M, Smith CJ, Bettinson H, Dart S, Bannister B, Johnson MA, et al. Paradoxical reactions during tuberculosis treatment in patients with and without HIV co-infection. Thorax 2004;59:704-7.
18. Tanaka T, Sekine A, Tsunoda Y, Takoi H, Lin S-Y, Yatagai Y, et al. Central nervous system manifestations of tuberculosis-associated immune reconstitution inflammatory syndrome during adalimumab therapy: a case report and review of the literature. Intern Med 2015;54:847-51.
19. Lynch K, Farrell M. Cerebral tuberculoma in a patient receiving anti-TNF alpha (adalimumab) treatment. Clin Rheumatol 2010;29:1201-4.
20. Minozzi S, Bonovas S, Lytras T, Pecoraro V, González-Lorenzo M, Bastiampillai AJ, et al. Risk of infections using anti-TNF agents in rheumatoid arthritis, psoriatic arthritis, and ankylosing spondylitis: a systematic review and meta-analysis. Expert Opin Drug Saf 2016;15:11-34.
21. Kim HW, Kwon SR, Jung K-H, Kim S-K, Baek HJ, Seo MR, et al. Safety of Resuming Tumor Necrosis Factor Inhibitors in Ankylosing Spondylitis Patients Concomitant with the Treatment of Active Tuberculosis: A Retrospective Nationwide Registry of the Korean Society of Spondyloarthritis Research. PLoS ONE 2016;11:e0153816.
22. Lee Y-M, Lee S-O, Choi S-H, Kim YS, Woo JH, Kim D-Y, et al. A prospective longitudinal study evaluating the usefulness of the interferon-gamma releasing assay for predicting active tuberculosis in allogeneic hematopoietic stem cell transplant recipients. J Infect 2014;69:165-73.
23. Poddubnyy D. Axial spondyloarthritis: is there a treatment of choice? Ther Adv Musculoskelet Dis 2013;5:45-54.
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe