Hidrogelurile sunt folosite des în biomedicină, dar, cel puțin până în prezent, materialele disponibile pentru realizarea lor au avut limitări esențiale. Unele geluri sintetice se degradează în timp, producând substanțe chimice toxice, iar unele geluri naturale nu sunt suficient de puternice pentru a susține fluxul sanguin arterial. O inovație importantă vine de la o echipă mixtă de bioinginerie medicală compusă din cercetători de la Harvard și MIT, dar și din Canada, Elveția, Germania și Arabia Saudită. Aceștia au creat un hidrogel unic, cu multiple utilizări în hemostază și vindecarea plăgilor. Testele preclinice arată că noul produs este rezistent, flexibil și biocompatibil (inofensiv pentru țesuturile vii). Bazat pe polipeptide și asemănător elastinei, hidrogelul obținut de cercetătorii de la Boston funcționează similar celorlalte hidrogeluri: se umflă în urma expunerii la apă. Conținutul de apă dă materialului o flexibilitate „gelatinoasă“, care imită proprietățile elastice ale țesutului uman (pielea sau vasele de sânge). Pe de altă parte, conținutul proteic (de polipeptide) adaugă forța substanței: când gelul este expus la lumina ultravioletă, se formează conexiuni puternice între moleculele de proteină (proces cunoscut în biomedicină drept „crosslinking“), care îi dau gelului stabilitate fără a mai fi necesară folosirea agenților chimici potențial toxici. Mecanismul de „crosslinking“ în prezența luminii este superior celui fizic, chimic sau enzimatic, deoarece compusul rezultat este stabil atât in vitro, cât și in vivo.
După ce gelul rezistent și flexibil își servește funcția în procesul de vindecare, enzimele eliberate în mod natural pot digera, treptat și complet, gelul fără efecte toxice. După ce gelul dispare, țesutul sănătos îi ia locul.
Deși cercetătorii s-au concentrat pe potențialul gelului ca ajutor în vindecarea rănilor, ei cred că poate fi folosit cu mai multe întrebuințări. „Hidrogelul nostru are mai multe indicații: poate fi utilizat ca structură de suport pentru creșterea celulelor, poate fi incorporat, alături de celule, într-un vas și injectat apoi pentru a stimula dezvoltarea țesuturilor“, a declarat Nasim Annabi, coautoare a cercetării. În plus, materialul poate fi folosit pentru etanșare, aderând la țesutul de la locul unei leziuni și creând o barieră peste rană.
Cercetătorii au arătat că pot ajusta proprietățile gelului pentru a controla forța sau expansiunea materialului și explorează alte posibile transformări pentru diferite aplicații specifice. Ar putea, de exemplu, să combine gelul cu nanoparticule de silicon, particule microscopice care s-au dovedit de succes în oprirea sângerării. „Asta ne-ar permite să oprim imediat sângerarea cu un singur tratament“, a adăugat Annabi, „există un potențial enorm pentru folosirea produsului în clinică. Metoda noastră este simplă, materialul este biocompatibil și sperăm să îl vedem curând rezolvând diferite probleme clinice“.
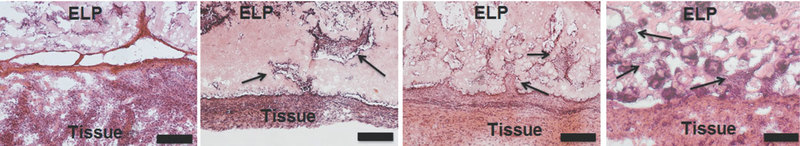
Pentru a testa stabilitatea și interacțiunea locală cu țesutul, precum și răspunsul imun al gazdei, cercetătorii au injectat subcutanat gelul la rozătoare. Probele prelevate în zilele 7, 14, 28 și 56 au arătat păstrarea macroscopică a formei implanturilor, fără a sugera o degradare relevantă. Colorația hematoxilin-eozină a arătat o creștere tisulară predominant noninflamatorie, ce confirma calitățile de biocompatibilitate și integrare in vivo. Lipsa degradării a fost analizată apoi in vitro prin incubarea hidrogelului cu proteinaza K pentru șase ore. Degradarea s-a produs în proporție de 20%. Degradarea lentă și creșterea tisulară sunt foarte utile, pentru că permit înlocuirea implantului cu țesut nou autolog. Histologic nu s-a găsit un infiltrat inflamator relevant, iar imunohistologic nu a fost găsit infiltrat limfocitar nici în implant, nici în țesutul subcutanat înconjurător.
In vitro, adăugarea de nanoparticule de dioxid de silicon ca soluție coloidală pe suprafața hidrogelului a scăzut timpul de coagulare pentru hidrogel cu până la 53%. In vivo, s-a realizat hemostaza în plăgi hepatice cu hemoragie acută, care altfel ar fi fost letale. Pierderea de masă sanguină este cu 76% și 94% mai mică după unul, respectiv zece minute, când sunt folosite combinat decât când hidrogelul este folosit singur. Adăugarea nanoparticulelor a scăzut timpul de sângerare la două minute, iar îndepărtarea materialului nu a produs resângerarea, astfel că sistemul și-a păstrat extensibilitatea și stabilitatea in vivo.
Cum hidrogelul dezvoltat a demonstrat in vivo o biocompatibilitate excelentă și o degradare minimă, cu creștere tisulară precoce din partea gazdei și cum îmbunătățirea lui funcțională cu nanoparticulele de dioxid de silicon a permis utilizarea lui eficientă într-o hemoragie letală hepatică, acesta are potențialul de a fi folosit în aplicații biomedicale pentru leziuni de țesuturi moi, flexibile precum vasele de sânge, pielea, plămânii sau inima. Rezultatele obținute la Boston au fost publicate în revista Advanced Functional Materials (Wiley).