În
ultimii 20 de ani, au avut loc mai multe tentative ministeriale de iniţiere a
unui program naţional de screening pentru cancerul colului uterin. Unele dintre
acestea au mers până la elaborarea şi publicarea de metodologii, de fiecare dată
concepute de novo, altele chiar până
la anunţarea publică a momentului implementării lor. Niciodată însă organizarea
unui astfel de program la nivel naţional nu a depăşit etapa de intenţie şi de
concepţie. Ultima metodologie, publicată în urmă cu câţiva ani, s-a soldat cu o
alertă generală printre potenţialii furnizori de servicii medicale clinice şi
de laborator dornici şi eligibili pentru un astfel de program, cu solicitarea
oficială de depunere în termen foarte scurt, la direcţiile de sănătate publică,
a unor dosare de participare, rămase apoi fără răspuns, şi cu mare agitaţie
printre furnizorii de consumabile care, inventivi şi aplicaţi, începuseră deja
să răspândească oferte de consumabile sub formă de „truse“ de recoltare şi de
colorare.
Circulă
din nou un zvon de bune intenţii privind programele de prevenţie… Dacă, de data
aceasta, zvonul se va adeveri şi într-adevăr va exista o finanţare rezonabilă
pentru o acţiune largă de medicină preventivă, cred că în modelarea acestui
program iniţiatorii ar trebui să ia în considerare cel puţin trei aspecte: • eşecul
programului de vaccinare anti-HPV în România • experienţa internaţională, dar
mai ales cea europeană – accesibilă şi concretizată într-un ghid de asigurare a
calităţii în screeningul pentru cancerul de col, recent revizuit sub egida
Consiliului Europei • progresele ştiinţifice şi tehnologia legate mai ales de
epidemiologia şi testarea infecţiei HPV, care au schimbat foarte mult modul
clasic de abordare a acestui tip de prevenţie.
Motivul
prezentării, în cele ce urmează, a câtorva considerente de specialitate îl
constituie dorinţa de a atrage atenţia decidenţilor şi responsabililor acestui
potenţial program de screening, în primul rând asupra faptului că mult aşteptata
şi atât de necesară măsură de sănătate publică în favoarea sănătăţii femeilor
are un specific multidisciplinar consacrat, indiferent de tipul testului
utilizat ca metodă de screening primar. De aceea, limitarea programului la
efectuarea testului Babeş-Papanicolaou, urmată de eliberarea unui bilet de
trimitere fără a se preciza încotro (pentru pacientele cu rezultate citologice
pozitive), aşa cum se menţionează în ultima metodologie accesibilă public, ar
constitui un start nefericit. Modul de
finalizare a diagnosticului, tratamentul cazurilor depistate, precum şi
supravegherea ulterioară a acestora sunt însăşi esenţa demersului preventiv.
În
al doilea rând, doresc să amintesc faptul că programele contemporane de luptă împotriva
cancerului de col ţintesc un orizont de timp mai lung şi integrează screeningul
(ca formă de prevenţie secundară focalizată pe găsirea şi îndepărtarea
precancerului de col) cu prevenţia primară, realizată prin vaccinarea generaţiei
tinere înainte de expunerea la virus, acţiune care are potenţialul de a reduce
incidenţa cancerului de col cu 75%. Această asociere este, din păcate, deja
compromisă la noi.
Fac
această pledoarie din perspectiva unei cariere personale îndelungate, practice şi
didactice, în patologia precanceroasă a colului uterin în România, precum şi
din cea a experienţei dobândite pe parcursul creării şi dezvoltării Clinicii
„Micomi“, centru medical privat specializat în patologia precanceroasă a
colului uterin, care dispune atât de expertiza umană complexă a unei echipei
medicale multidisciplinare dedicate, cât şi de tehnologia medicală de vârf în
domeniu.
Pentru
a ilustra amploarea experienţei în citopatologie (una din competenţele
noastre), notez numărul de peste 300.000 de frotiuri citologice pe care
„Micomi“ le-a procesat şi interpretat în ultimii ani şi la care s-au formulat
recomandări personalizate de conduită.
Screeningul bazat pe testul citologic Babeş-Papanicolaou
Programele
clasice de screening cervical bazat pe citologie rămân cel mai de succes model
de prevenţie a unei forme de cancer. Succesul este dat, practic, de incidenţa
scăzută a cancerului de col invaziv în populaţiile cu screening, faţă de ratele
înalte ale incidenţei şi mortalităţii prin această boală în populaţiile fără
screening.
În
scenariul clasic, testul primar este citologia Babeş-Papanicolaou, iar ţinta
este identificarea şi îndepărtarea leziunilor precursoare de cancer, mai ales a
modificărilor ce apar pe linie scuamoasă (respectiv CIN III/displazia severă şi
carcinomul in situ), care sunt
curabile şi prin eradicarea cărora se întrerupe procesul de degenerare în
cancer.
Rezultatele citologice pozitive, care
reprezintă 5–8% din totalul rezultatelor unui screening, sunt apoi investigate
suplimentar, începând cu o evaluare colposcopică. În funcţie de aceasta, prin
corelare cu vârsta şi antecedentele pacientei, urmează aplicarea fie a unei
proceduri de biopsiere, fie a unui algoritm de supraveghere. Rezultatul
histopatologic decide apoi dacă este cazul să se recurgă la un tratament
conservator excizional (de regulă pentru leziuni intraepiteliale cu severitate
de la CIN II/displazie moderată în sus, dar, în anumite situaţii clinice, şi
pentru CIN I/displazie simplă), cu grijă pentru evitarea supradiagnosticului şi
restricţionarea de principiu a tratamentului la leziunile intraepiteliale de
grad înalt. Studii recente arată că supravegherea pacientelor tratate pentru o
leziune precanceroasă de grad înalt trebuie să continue 20 de ani, cu o frecvenţă
mai mare în primii doi ani postoperator, când sunt mai frecvente leziunile
restante sau recidivate. Cazurile de carcinom invaziv (în jurul unui procent
din totalul rezultatelor din screening) se îndrumă către reţeaua de oncologie.
principiu a tratamentului la leziunile intraepiteliale de
grad înalt. Studii recente arată că supravegherea pacientelor tratate pentru o
leziune precanceroasă de grad înalt trebuie să continue 20 de ani, cu o frecvenţă
mai mare în primii doi ani postoperator, când sunt mai frecvente leziunile
restante sau recidivate. Cazurile de carcinom invaziv (în jurul unui procent
din totalul rezultatelor din screening) se îndrumă către reţeaua de oncologie.
Prin urmare, pentru elucidarea unui rezultat
citologic anormal sau echivoc este nevoie de o expertiză clinică
(ginecologie/colposcopie pentru diagnostic şi tratament excizional sau
chirurgical), de una histopatologică, uneori completată de teste de
imunohistochimie, şi de una de biologie moleculară, utilitatea clinică a testării
HPV în screening fiind în prezent bine definită. Fiecare pas al procesului de
screening clasic (citologia, colposcopia şi histopatologia) are o componentă
umană subiectivă, care ţine în mare măsură de specializare şi de experienţă,
dar care aduce, inerent, unele limitări în ceea ce priveşte sensibilitatea şi
specificitatea faţă de CIN III, adevăratul precursor de cancer. Pentru a
compensa limitele fiecărei metode, practic pentru a reduce rata diagnosticului
fals negativ al precancerului, în special la nivelul testului citologic iniţial,
programele clasice de screening recurg la diferite soluţii, dintre care cele
mai deosebite sunt instituirea unui protocol intern riguros de control al calităţii
în laboratorul de citopatologie şi coborârea ţintei de tratament la CIN II, ca
măsură de siguranţă suplimentară, chiar dacă această modificare are şanse
importante de regresie spontană.
Se apreciază că un singur test citologic în
viaţă are o sensibilitate de numai 50% pentru detectarea leziunilor
precanceroase. În schimb, repetarea citologiei la fiecare trei ani previne 90%
din cancerele care ar apărea în absenţa screeningului. De aceea, pentru ca
citologia cervicală utilizată ca metodă de screening primar să atingă un nivel
cât mai înalt de sensibilitate şi implicit de eficienţă, pe lângă investigarea
suplimentară a tuturor pacientelor cu rezultate citologice anormale, inclusiv a
celor cu modificări citologice minore persistente, este nevoie în primul rând
de repetarea regulată a testului cu rezultat negativ pentru o leziune
intraepitelială sau malignă, la intervale bine definite.
Faptul că citologia nu este un test perfect,
adică are o inerentă proporţie de rezultate fals pozitive şi fals negative,
este însă o informaţie dificil de comunicat pacientelor şi greu de înţeles
chiar de către cele foarte instruite. Informarea publică nepotrivită asupra
acestui aspect esenţial poate scădea încrederea în program, poate demobiliza
femeile care ar dori să participe la screening, sau poate diminua complianţa faţă
de recomandările de investigaţii suplimentare. De asemenea, contează foarte
mult modul în care informaţia este transmisă femeilor direct de personalul
medical implicat în momentul recomandării unei citologii, în cazul unui
rezultat cu probleme, înainte de efectuarea unei colposcopii ori intervenţii
sau când trebuie comunicat un diagnostic de cancer. Comunicarea şi consilierea
sunt părţi esenţiale ale unui program de screening.
Repetarea
regulată a citologiei a condus la o scădere de peste 70% în mortalitatea prin
cancerul cervical în ţările dezvoltate, care dispun de resurse suficiente
pentru a susţine programe de screening organizate la nivel populaţional şi de o
infrastructură cu sisteme de control al calităţii activităţii medicale la toate
nivelele bine pus la punct. Cancerul de col continuă însă să fie o problemă
importantă de sănătate publică în ţările în curs de dezvoltare, unde incidenţa şi
mortalitatea rămân foarte mari. Astfel, 85% din aproximativ jumătate de milion
de cazuri noi care se înregistrează anual în lume apar în aceste ţări şi se
estimează că în anul 2030 această proporţie va ajunge de 90%.
În
Europa sunt raportate anual 34.000 de cazuri noi şi 16.000 de decese. Rata cea mai înaltă a mortalităţii
standardizate se înregistrează în România şi Lituania (13,7, respectiv
10/100.000 de femei), iar cea mai scăzută în Finlanda (1,1/100.000).
Experţii
internaţionali în sănătate publică consideră că replicarea în ţările emergente
a modelului de screening clasic descris mai sus nu funcţionează în special din
lipsa resurselor necesare pentru dezvoltarea infrastructurii medicale specifice
acestui program, care să asigure buna organizare, coordonare şi monitorizare,
un protocol standard multidisciplinar cuprinzător, repetat regulat, cu vizite
multiple, un personal medical dedicat şi bine instruit (care să ştie şi să poată
lucra în echipă multidisciplinară), accesibilitatea şi o activitate de educaţie
publică susţinută. Acestor ţări li se propun programe de screening care
folosesc anumite metode zise alternative, pe care şi le pot permite din punct
de vedere financiar şi care nu presupun un anume nivel de dezvoltare a
infrastructurii serviciilor medicale, cum ar fi inspecţia vizuală cu acid
acetic (VIA) asociată cu crioterapia, pe care le consider fără aplicabilitate într-o
ţară europeană ca România.
În
Uniunea Europeană există ţări cu programe organizate de screening, dar şi multe
state cu abordări oportuniste – unele dintre ele fac în prezent schimbări în
privinţa tipului de teste şi a tehnologiilor aplicate pe baza unor studii ample
de cost-eficienţă; toate aceste ţări au însă rate foarte scăzute ale mortalităţii
prin cancer de col. România, care înregistrează cea mai înaltă rată a mortalităţii
prin cancer de col uterin din această regiune, trebuie să ia în sfârşit o
decizie asupra aplicării unui protocol de depistare şi rezolvare a cazurilor
identificate.
Controlul intern al calităţii în laboratoarele de
citopatologie
Indiferent
de abordarea populaţională sau oportunistă a screeningului, toate laboratoarele
de citopatologie din Europa – ca de altfel şi cele specializate din restul
lumii – funcţionează pe baza unor protocoale riguroase pentru controlul intern
al calităţii. Acest control are ca scop reducerea la minimum a procentului de
rezultate fals negative.
Variaţia
părerilor interobservatori, în special la limita între un rezultat negativ cu
modificări reactive şi un rezultat cu minime modificări nucleare clasificate
ASC-US (atypical squamous cells of
undetermined significance), generată de existenţa unor elemente subiective în
aprecierea individuală a cazurilor, se poate rezolva numai prin discutarea
acestor situaţii în reuniuni de lucru regulate, în cadrul laboratorului.
Ideal,
controlul de calitate constă în examinarea tuturor frotiurilor în mod
independent, de două persoane competente. Acest lucru se practică sub forma
citirii sau revederii rapide, în sistemul britanic de screening. În cel
american, este obligatorie recitirea aleatorie a 10% din rezultatele negative. În
funcţie de volumul de lucru, acest procent variază, în alte forme de
organizare.
Alte
procedee consacrate ale controlului intern sunt: citirea frotiurilor aparţinând
unor paciente cu risc direct de către anatomopatolog, revederea de rutină a
frotiurilor apreciate anterior ca negative la cazurile la care citologia sau
biopsia actuală este pozitivă, monitorizarea rezultatelor ASC-US, care nu
trebuie să depăşească 5% din totalul citologiilor efectuate de laboratorul
respectiv, compararea rezultatelor citologice cu cele colposcopice şi histopatologice,
compararea rezultatelor ASC-US cu rezultatele testării HPV.
Procedeul
cel mai eficient în stabilirea conduitei medicale adecvate la cazurile-problemă
sau cu aspecte echivoce este discutarea lor în întâlniri multidisciplinare. În
servicii medicale neintegrate sau necoordonate într-un program de screening, întrunirea
specialiştilor respectivi este, practic, imposibilă.
 Toate
aceste măsuri presupun, evident, informatizarea laboratorului şi un volum crescut
de muncă pentru evaluarea propriu-zisă a frotiurilor citologice, o intensă
activitate managerială referitoare la evidenţa şi organizarea acestei activităţi,
precum şi organizarea şi menţinerea unei lamoteci şi a unei arhive.
Toate
aceste măsuri presupun, evident, informatizarea laboratorului şi un volum crescut
de muncă pentru evaluarea propriu-zisă a frotiurilor citologice, o intensă
activitate managerială referitoare la evidenţa şi organizarea acestei activităţi,
precum şi organizarea şi menţinerea unei lamoteci şi a unei arhive.
Acestea
sunt unele dintre motivele pentru care consider că un singur „cititor“ de
frotiuri, fie el biolog sau medic de laborator cu formare în citologie, dar cu
responsabilităţi curente în specialitatea sa, oricât de performant ar fi, nu
poate îndeplini o muncă de calitate în citopatologie dacă nu este integrat într-un
laborator dedicat, cu sistem organizat de control intern şi extern al calităţii
şi coordonat de anatomopatologi.
Progresele tehnice în recoltarea, prelucrarea şi
interpretarea frotiurilor citologice
Pe de altă parte, trebuie luat în
considerare şi faptul că citologia a cunoscut, în ultimii ani, importante progrese
tehnice, care elimină erorile de recoltare. Ele se referă la înlocuirea recoltării
cu etalare convenţională cu cea în mediu lichid, urmată de transferarea
celulelor pe lamă prin diverse procedee automate sau semiautomate, în strat subţire
sau monostrat. Citologia în mediu lichid, deşi atunci când este citită manual
are o acurateţe comparabilă cu citologia convenţională în identificarea
leziunilor precanceroase, aduce avantaje importante atât pentru clinician şi
pacientă (pentru că se soldează cu mult mai puţine rezultate nesatisfăcătoare),
cât şi pentru citologi şi citopatologi (care au de interpretat o suprafaţă de
frotiu mai mică şi uniform etalată). Ea permite, totodată, efectuarea simultană
sau ulterioară a unor teste suplimentare – cum sunt cele pentru HPV, Chlamydia şi gonococ – din lichidul rezidual
al aceleiaşi recoltări.
În fine, procedeul cel mai performant de
asigurare a calităţii laboratorului de citopatologie, pe care îl utilizăm şi la
„Micomi“ în cadrul controlului intern al calităţii laboratorului pentru
citologia recoltată în mediu lichid, este cel care dublează expertiza umană de
precitirea robotizată a frotiurilor. Acest procedeu preselectează, printr-un
program informatic specializat, un anumit număr de câmpuri microscopice
reprezentative. Interpretarea acestora şi formularea rezultatului citologic rămân
însă în sarcina specialiştilor în citologie.
Indicaţiile testării
HPV
Orice program contemporan de prevenţie a
cancerului de col nu poate ignora rolul şi utilitatea testării HPV. Indicaţiile
de recurgere la acest test suplimentar au apărut la începutul anilor 2000, ca
posibilitate de triaj înainte de colposcopie a unui număr de aproximativ 5% din
totalul rezultatelor citologice (respectiv, a celor cu aspect citologic
echivoc, etichetate ASC-US). Doar aproximativ 50% din rezultatele citologice
interpretate ASC-US au drept cauză o infecţie HPV cu risc înalt, care impune
investigaţii suplimentare. Testarea evită excesul de proceduri excizionale al căror
impact negativ asupra fertilităţii ulterioare este dovedit.
Indicaţiile testării HPV s-au extins în
scurt timp, până la dublarea citologiilor în screeningul primar, la femei peste
30 de ani, ca mijloc de obţinere a unei predictibilităţi superioare a
leziunilor cervicale, faţă de screeningul exclusiv citologic.
Asocierea testării HPV cu risc înalt cu
citologia (cotestarea) în screening la femeile peste 30 de ani (vârstă la care
incidenţa infecţiei virale este în scădere, în schimb incidenţa cancerului de
col creşte) aduce informaţii suplimentare valoroase faţă de cele oferite
exclusiv de citologie. Cotestarea permite lărgirea intervalului de supraveghere
la persoanele cu ambele teste negative (care menţin un risc scăzut pentru
leziuni precanceroase sau cancer pentru mai mulţi ani) şi concentrarea atenţiei
asupra persoanelor cu citologie negativă şi test HPV pozitiv.
Mai mult decât atât, testarea HPV este, în
prezent, preferată metodelor clasice şi în supravegherea postoperatorie a
leziunilor precanceroase, când este considerată marker de vindecare.
Studii recente au demonstrat faptul că riscul
pentru leziuni cervicale nu este egal pentru oricare din tipurile de HPV din
grupul cu risc, ci, dimpotrivă, că identificarea riscului legat de genotipurile
cele mai agresive (16 şi/sau 18) contribuie la selectarea şi tratarea precoce a
unui număr mai mare de leziuni precanceroase. Pacientele pozitive pentru HPV 16
şi/sau 18 trebuie trimise direct pentru evaluare colposcopică, chiar dacă
rezultatul examenului lor citologic este negativ.
Modele de metodologie în programele moderne de screening
Recomandările europene privind screeningul
pentru cancerul cervical (European
guidelines for quality assurance in cervical cancer screening), bazate pe
dovezile din literatura de specialitate, au fost elaborate în cadrul
programului „Europa împotriva cancerului“, de o echipă multidisciplinară de 48
de specialişti, sub forma unei adevărate monografii de 250 de pagini, publicată
în 2008 şi revizuită în 2010. Acest ghid cuprinde principii şi standarde,
aspectele tehnice esenţiale, măsurile de asigurare a calităţii de la recoltare
la prelucrarea probelor în laboratorul de citologie şi histopatologie, precum şi
criteriile clinice de evitare a supradiagnosticului şi supratratamentului.
Sunt, de asemenea, propuşi indicatori uniformi de monitorizare a performanţei
programului, de identificare şi reacţie la timp faţă de problemele potenţiale,
care să permită comparabilitatea datelor, schimbul de experienţă şi informaţii între
diferitele programe de screening din Europa. Ghidul recomandă ţărilor care nu
au lansat încă programe de screening să acţioneze pe baza recomandărilor şi
standardelor europene, care se adresează atât prevenţiei primare, cât şi celei
secundare.
Ghidul european are numai diferenţe de nuanţă
faţă de cel american, în capitolul referitor la managementul rezultatelor
citologice anormale. În rest, criteriile de control al calităţii sunt identice şi
trebuie luate drept model, dacă dorim să construim în România un program
viabil, eficient şi cost-eficient pe termen lung.
Perspective: screening primar HPV, biomarkeri
Privind lucrurile din perspectiva generalizării
vaccinării profilactice HPV, care va scădea spre zero numărul leziunilor
precanceroase induse de HPV 16 şi/sau 18, precum şi prevalenţa infecţiei
virale, multe personalităţi ştiinţifice internaţionale autorizate demonstrează
astăzi că eficienţa screeningului citologic va scădea simţitor la persoanele
vaccinate şi pledează pentru schimbarea totală a conceptului clasic de
screening, cu inversarea ordinii în care se utilizează în prezent cele două teste.
Aceşti experţi susţin o metodologie în care
testul de screening iniţial să fie cel pentru ADN HPV, cu repetare la un
interval de trei-cinci ani. Citologia ar funcţiona atunci ca test de triaj al
cazurilor HPV pozitive, urmând ca investigaţiile clasice cu colposcopie şi
biopsie să se efectueze numai la pacientele cu testare HPV pozitivă care se
asociază cu citologie modificată. Schimbarea istorică constă, de fapt, în
combinaţia inteligentă dintre vaccinarea generalizată şi organizarea unor
protocoale de screening mai eficiente. Însă trecerea de la programele curente
la protocoale de screening bazate pe vaccinare şi testare HPV se dovedeşte
pentru moment a fi dificilă, chiar şi în ţările cu tradiţie în screening.
Între timp, lumea ştiinţifică internaţională
oferă noi orizonturi în prevenţia secundară. Se dezvoltă, se testează şi se ni
se propun noi biomarkeri, ca metode de screening primar, între care cei mai
studiaţi sunt P16INKA şi ARN mesager. Aplicabilitatea lor ca metode
de screening necesită în continuare studii de confirmare.
Componenta clinică a unui program de screening
Evaluarea sensibilităţii şi specificităţii
diferitelor teste şi procedee utilizate ca metode de prevenţie şi diagnostic în
precancerul de col arată că niciuna dintre acestea nu este perfectă. De aceea,
pentru stabilirea unei conduite medicale cât mai adecvate şi protective la caz,
este esenţială evaluarea riscului individual pentru leziuni cervicale. Acesta
este cu atât mai corect cuantificabil, cu cât pacienta a efectuat mai mult de
un tip de investigaţii care evaluează colul uterin. Riscul trebuie exprimat
suficient de inteligibil, în rezultatele de citologie şi/sau testare HPV.
În cazul când, din screening, se selectează
paciente cu leziuni cervicale induse de HPV, evaluarea şi personalizarea
riscului acestora, ca şi evitarea supratratamentului, se realizează de medicii
care practică aşa-numita „colposcopie integrată“, prin corelarea rezultatelor
investigaţiilor cu anamneza, aspectul colposcopic şi cu celelalte date clinice.
Acest lucru este relevant numai cu condiţia ca investigaţiile care se integrează
să se fi desfăşurat într-un laborator dedicat, care îşi menţine standardul prin
aplicarea coerentă, continuă şi riguroasă a măsurilor interne specifice de
asigurare a calităţii.
Colposcopia, competenţă suplimentară a
medicilor ginecologi, cu acelaşi risc al interpretării umane ca şi
cito-/histopatologia, rămâne placa turnantă în diagnosticul, tratamentul şi
supravegherea precancerului de col uterin. Toate ghidurile de practică acceptă
faptul că, atunci când ajungem la rezolvarea unui caz individual, selectat sau
nu dintr-un program screening cu un bun control la toate nivelurile, recomandările
din ghiduri pot să nu acopere marea variabilitate a situaţiilor clinice, conduita
adoptată fiind cea asupra căreia cad de acord medicul curant şi pacienta.
Ginecologii care îngrijesc paciente cu
patologie cervicală ştiu că evoluţia naturală a infecţiei HPV este foarte
variabilă, ca şi riscul de boală indusă de HPV şi răspunsul la tratament – de
asemenea, diferite de la persoană la persoană. Astfel, numai o mică parte din
persoanele infectate cu HPV ajung să dezvolte cancerul cervical, în timp ce
majoritatea infecţiilor se rezolvă spontan; anumite infecţii virale au o evoluţie
ondulatorie intermitentă, multe sunt infecţii multiple, unele au localizare
multifocală, numai unele leziuni precanceroase regresează şi, câteodată,
constatăm că boala canceroasă evoluează foarte rapid. Aceste lucruri,
binecunoscute în practica clinică, se explică astăzi prin existenţa unor variaţii
la nivelul codului genetic uman, prin faptul că, pe parcursul vieţii, anumite
gene interacţionează cu factori din mediul înconjurător, precum şi amprentei
unice, individuale a sistemului nostru imun.
Componenta clinică de
ginecologie-colposcopie nu poate lipsi dintr-un program de screening. Pe de altă
parte, ca orice program de screening, nici cel pentru cancerul de col uterin
nu se poate derula şi monitoriza fără implicarea medicilor de familie. Măsura şi
condiţiile în care aceştia doresc să participe este de asemenea de ştiut.
Tipul de conexiuni profesionale între
specialiştii implicaţi şi între verigile instituţionale ale programului de
screening, respectarea dreptului pacientelor de a alege medicul şi locul pentru
recoltarea, procesarea şi interpretarea probelor, pentru colposcopie şi
tratament, coordonarea profesională şi administrativă, inclusiv ritmul şi
limitele de vârstă ale pacientelor ce pot intra în program sunt alte aspecte
care trebuie discutate şi clarificate înainte de a lansa programul de
screening.
Să sperăm că zvonul amintit mai sus se va
adeveri şi că programul de screening se va croi în spiritul ştiinţific al
secolului 21. Trăim totuşi în ţara în care Aurel Babeş a descris pentru prima
dată în lume rolul frotiului citologic în patologia colului uterin. După 84 de
ani de la publicarea articolului lui Babeş în La Presse Médicale, mortalitatea prin cancer al colului uterin în ţara
noastră – în mare măsură evitabilă – este cea mai mare din Europa. Acesta este,
în fapt, motivul incontestabil pentru care screeningul pentru cancerul de col
uterin constituie o problemă prioritară de sănătate publică în România. Problemă
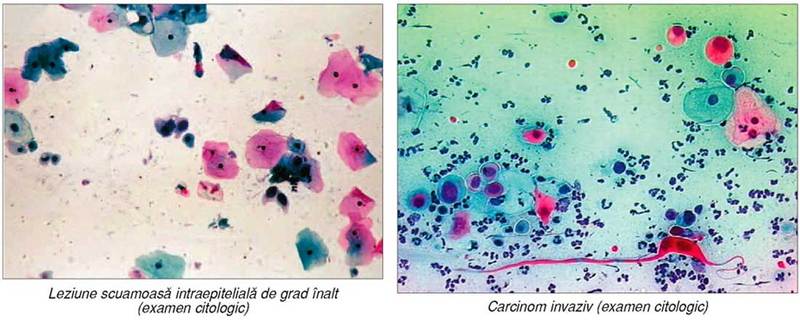
ce trebuie considerată şi tratată ca atare de decidenţii politici. Ilustraţiile provin din arhiva Clinicii „Micomi“ Bucureşti
 principiu a tratamentului la leziunile intraepiteliale de
grad înalt. Studii recente arată că supravegherea pacientelor tratate pentru o
leziune precanceroasă de grad înalt trebuie să continue 20 de ani, cu o frecvenţă
mai mare în primii doi ani postoperator, când sunt mai frecvente leziunile
restante sau recidivate. Cazurile de carcinom invaziv (în jurul unui procent
din totalul rezultatelor din screening) se îndrumă către reţeaua de oncologie.
principiu a tratamentului la leziunile intraepiteliale de
grad înalt. Studii recente arată că supravegherea pacientelor tratate pentru o
leziune precanceroasă de grad înalt trebuie să continue 20 de ani, cu o frecvenţă
mai mare în primii doi ani postoperator, când sunt mai frecvente leziunile
restante sau recidivate. Cazurile de carcinom invaziv (în jurul unui procent
din totalul rezultatelor din screening) se îndrumă către reţeaua de oncologie. Toate
aceste măsuri presupun, evident, informatizarea laboratorului şi un volum crescut
de muncă pentru evaluarea propriu-zisă a frotiurilor citologice, o intensă
activitate managerială referitoare la evidenţa şi organizarea acestei activităţi,
precum şi organizarea şi menţinerea unei lamoteci şi a unei arhive.
Toate
aceste măsuri presupun, evident, informatizarea laboratorului şi un volum crescut
de muncă pentru evaluarea propriu-zisă a frotiurilor citologice, o intensă
activitate managerială referitoare la evidenţa şi organizarea acestei activităţi,
precum şi organizarea şi menţinerea unei lamoteci şi a unei arhive.