FDA a aprobat, la 8 decembrie, primele două terapii genice pentru siclemie. Unul dintre aceste tratamente este primul aprobat care folosește tehnologia de editare genică CRISPR/Cas9.
Noile terapii pentru siclemie (anemia cu celule în seceră) sunt destinate pacienţilor cu vârsta de cel puţin 12 ani. În prezent, persoanele afectate de această boală au la dispoziţie tratamente analgezice sau care vizează tratarea sau prevenirea complicaţiilor, cum ar fi crizele vasoocluzive. Însă cele două sunt primele care corectează defectul genetic moștenit.
Ambele terapii sunt personalizate și create pe baza celulelor stem hematopoietice ale pacientului. Aceste celule sunt recoltate din măduva osoasă, modificate și apoi administrate pacientului în perfuzie, într-o unică ședinţă. În prealabil, pacienţii primesc doze mari de chimioterapie menite să elimine celulele defecte, măduva osoasă urmând a fi repopulată cu celulele corectate.
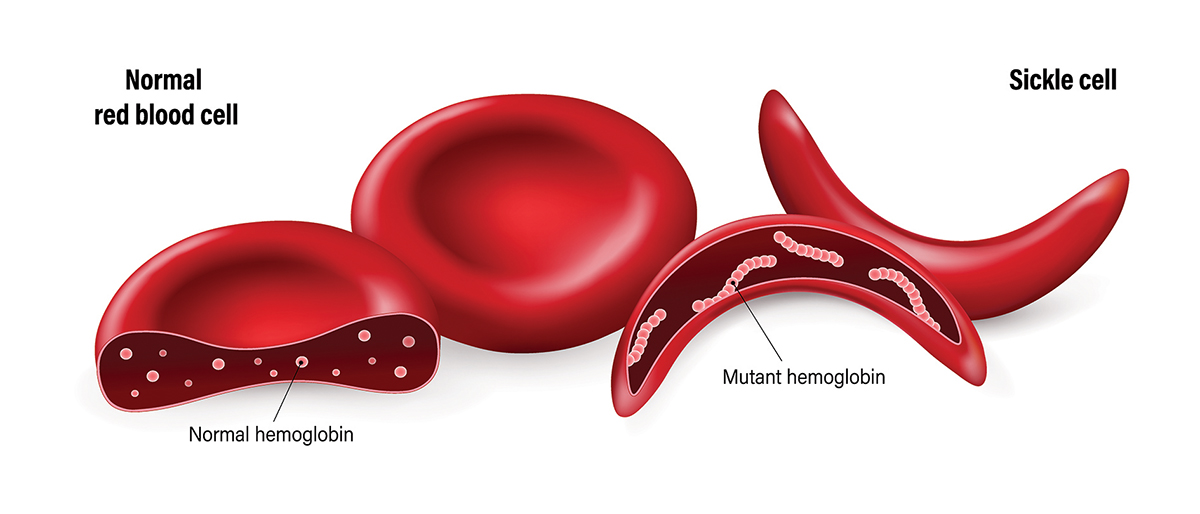
Siclemia sau anemia cu celule în seceră este o boală rară, gravă, transmisă genetic, în care organismul persoanelor afectate produce un tip anormal de hemoglobină, HbS. Hematiile ce conţin aproape 100% HbS iau forma de seceră și sunt rigide, ceea ce perturbă atât fluxul sanguin, cât și schimbul de gaze din ţesuturi.
Una dintre terapiile aprobate folosește un vector viral și a fost aprobată pentru tratarea pacienţilor cu istoric de crize vasoocluzive. Cu ajutorul acestor lentivirusuri, celulele stem sunt modificate genetic pentru a produce o hemoglobină nouă, HbATb7Q, care funcţionează precum HbA. Hematiile care conţin HbATb7Q au o probabilitate mai mică de a se „îndoi” și de a lua formă de seceră.
Terapia pe bază de CRISPR/Cas9 modifică celulele hematopoietice prin tehnici de reparare a ADN-ului, astfel încât acestea să producă mai multă hemoglobină fetală (HbF). Studiile clinice au arătat că pacienţii astfel trataţi au avut cel puţin 12 luni consecutive lipsite de crize vasoocluzive în cei doi ani de monitorizare.
Cele mai frecvente efecte adverse au fost scăderea numărului de trombocite și leucocite, stomatită, greaţă și vomă, dureri musculoscheletale, abdominale, cefalee și prurit. Tratamentul pe bază de vector viral a obţinut rezultate similare, dar s-a asociat și cu apariţia cancerului de sânge la unii pacienţi. De aceea, prospectul său include această avertizare.
https://www.fda.gov/news-events/press-announcements/fda-approves-first-gene-therapies-treat-patients-sickle-cell-disease
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe