
De Ziua Internaţională a Studiilor Clinice, reprezentanţi ai autorităţilor, industriei farma și ai CRO au punctat pașii pe care România îi are de făcut pentru a relansa domeniul studiilor clinice pentru ţara noastră.
Chirurgul scoţian James Lind realiza, la 20 mai 1747, primul experiment pe subiecţi umani, considerat drept primul studiu clinic din istorie. Era perioada în care foarte mulţi oameni se îmbolnăveau de scorbut, din cauza aportului insuficient de vitamina C. Aflat la bordul Navei Regale Britanice Salisbury, dr. James Lind a încercat să trateze această boală, de care sufereau majoritatea marinarilor, prin administrarea a diferite remedii. Cei cărora le-a administrat câte două portocale și o lămâie zilnic au avut cea mai spectaculoasă revenire și efecte vizibile de îmbunătăţire a stării lor, „the most sudden and good visible effect”, după cum scria chiar Lind în raportul de studiu.
Practic, experimentul lui Lind este recunoscut ca fiind fundamentul cercetării clinice moderne. Astfel că în anul 2005 s-a propus ca ziua de 20 mai să fie recunoscută ca Ziua Internaţională a Studiilor Clinice, zi sărbătorită de comunitatea medicală de cercetare clinică din întreaga lume de atunci până în prezent.
Tot la 20 mai, Avantyo Institute of Clinical Research a organizat în România, cu ocazia acestei zile, o masă rotundă de discuţii despre implementarea Regulamentului European 536/2014 – un subiect extrem de important și sensibil, cu atât mai mult cu cât, în numai opt luni, noul regulament va intra în vigoare. Începând din ianuarie 2022, orice studiu clinic ce se va desfășura în centre de înrolare medicale din Europa va trebui înregistrat într-un singur sistem informatic, CTIS (clinical trial information system), și în același mod pentru absolut toate centrele de studiu din toate ţările membre UE.
Invitaţi din străinătate au fost dr. Martine Dehlinger Kremer, președinte EUCROF, și dr. Ingrid Klingmann, președinte EFGCP (European Forum for Good Clinical Practice).
Discuţia liberă s-a concentrat în prima parte pe contextul internaţional, astfel că s-au trecut în revistă modificările aduse de noul regulament al studiilor clinice comparativ cu vechea directivă europeană de studii clinice. Am aflat că la nivelul Comisiei Europene există o hartă a celor 27 de state membre unde se urmărește foarte atent modul în care fiecare își pregătește tranziţia către noul regulament. Vorbim astfel despre un fel de semafor în culorile verde, galben și roșu:
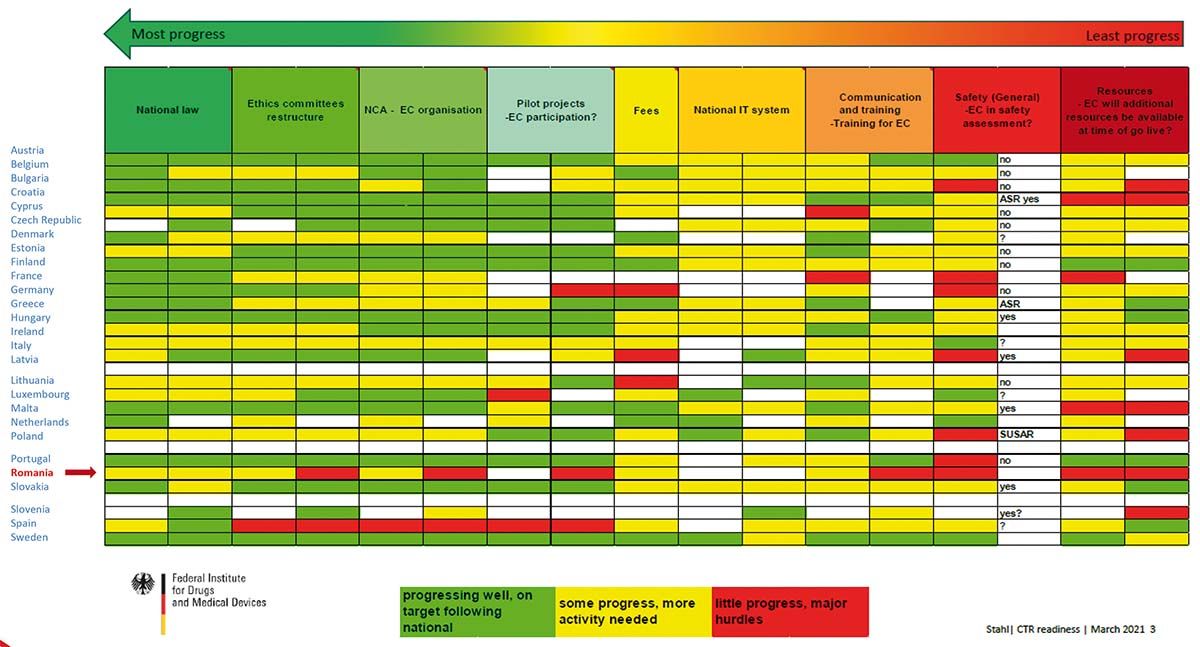
Concluzia primului panel de discuţii a fost că CTR 536/2014 aduce armonizarea în procedura de submitere și aprobare la nivelul tuturor statelor membre, existând o singură submitere de documente, un singur hub electronic unde acestea se înregistrează – sistemul CTIS –, un singur număr alocat studiului, o singură procedură de evaluare, o singură decizie privind aprobarea, o singură taxă de plătit.
Am dorit ca întâlnirea noastră să fie una în care să auzim soluţii practice pe care autorităţile române le au în vedere pentru adoptare în perioada imediat următoare. Și vă pot spune că per total, panelul al doilea de discuţii, „Status Quo România in implementation CT Regulation 536/2014 for harmonization of CT authorization”, a adus vești bune, termene de urmărit și multă speranţă.
Astfel, dr. Roxana Stroe, președintele ANMDMR, ne-a anunţat că în acest moment se pregătește organizarea concursului la ANMDMR pentru ocuparea posturilor vacante, inclusiv în cadrul departamentului de studii clinice, precum și a concursului pentru ocuparea postului de președinte și vicepreședinte al agenţiei. În același timp, ca urmare a unui ordin al Ministerului Sănătăţii (MS) recent publicat, se va organiza un grup de lucru constituit din reprezentanţii ANMDMR, Comisiei de Bioetică și MS pentru discutarea implementării CTR 536/2014 în ţara noastră, cu pași și termene clare de stabilit.
În iunie și iulie 2021 vor avea loc discuţii ale autorităţilor cu reprezentanţii farma și ai CRO-urilor, pentru a analiza toate propunerile legislative ale acestora, făcute încă din octombrie 2020 către autorităţi. Și aici aș menţiona doar câteva:
În numele transparenţei și al informării cetăţenilor interesaţi a participa în studii clinice, regulamentul menţionează că sunt admise scurte reclame în mass-media, cu un minimum de informaţii despre un studiu clinic (cf. Art. 60 din Anexa 1 lit. K), pe orice suport (scris, vorbit, video). Acest lucru trebuie de asemenea adoptat în legislaţia noastră naţională.
Avem promisiunea că în luna septembrie 2021 ANMDMR va înainta MS un draft pentru un nou ordin de ministru sau lege care să transpună noul regulament de studii în legislaţia naţională și care să delimiteze clar ce va avea de făcut ANMDMR și ce va avea de făcut Comisia de Bioetică în faţa unui studiu clinic nou submis spre revizuire și aprobare.
Președintele Comisiei de Sănătate din Senat, prof. dr. Adrian Streinu Cercel, și secretarul de stat în Ministerul Sănătăţii, Monica Althamer, ne-au asigurat că, în momentul în care acest draft de iniţiativă legislativă va fi adus în atenţia lor, revizuirea cu aprobarea și publicarea lui se vor putea face la nivel de săptămâni.
O altă veste foarte importantă a fost aceea că la nivelul Registrului Naţional de Educaţie s-a primit avizul pentru organizarea unui master de studii clinice în cadrul Facultăţii de Farmacie, sub formă de curs postuniversitar de pregătire ca specialist în acest domeniu, ceea ce într-un viitor apropiat va însemna aducerea de noi specialiști care să lucreze în ANMDMR. Sperăm ca acest lucru să rezolve problema veche a lipsei de personal a acestei instituţii și mai ales a departamentului de studii clinice.
Cu această ocazie, a sărbătoririi Zilei Internaţionale a Studiilor Clinice, doresc să le transmit aprecierea noastră miilor de specialiști din acest domeniu (medici, asistenţi medicali, farmaciști și alţii) care au decis să aleagă această carieră atât de frumoasă și și-au dedicat eforturile în găsirea de soluţii inovatoare de tratament care să îmbunătăţească sănătatea publică la nivel
mondial.
De asemenea, astăzi doresc să transmit un foarte mare MULŢUMESC tuturor voluntarilor și pacienţilor participanţi în studii clinice – contribuţia lor la știinţă este de nepreţuit. Înţelegem astfel cu toţii că doar împreună vom putea să facem o reală diferenţă în viaţa oamenilor.
Citește și:
https://www.radioromaniacultural.ro/stiinta-360-ziua-internationala-a-studiilor-clinice/
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe