
Sunt încă în dezbatere metodele ideale de diagnostic pentru depistarea infecţiei cu H. pylori, necesitatea culturilor și antibiogramei înainte de prescrierea tratamentului, schema de tratament pe care trebuie să o alegem, precum și metoda de confirmare a eradicării.
 Helicobacter pylori (H. pylori) este o bacterie Gram negativă care colonizează corpul și antrul gastric, cu transmitere fecal-orală, capabilă să supravieţuiască mediului acid gastric. Infecţia cu H. pylori rămâne una dintre cele mai comune infecţii bacteriene cronice care afectează oamenii, având o prevalenţă globală de aproximativ 50%.
Helicobacter pylori (H. pylori) este o bacterie Gram negativă care colonizează corpul și antrul gastric, cu transmitere fecal-orală, capabilă să supravieţuiască mediului acid gastric. Infecţia cu H. pylori rămâne una dintre cele mai comune infecţii bacteriene cronice care afectează oamenii, având o prevalenţă globală de aproximativ 50%.
Ratele cele mai mari de infectare se regăsesc în regiunile cu un statut socio-economic scăzut, cu un maxim al prevalenţei în Africa (70,1%, 95% CI, 62,6-77,7) și un minim în Elveţia (18,9%, 95% CI 13,1-4,7).
În România există puţine date disponibile din studii epidemiologice, mai ales conduse la nivel naţional. Într-un studiu publicat în 2003 de Sporea et al. s-a raportat o prevalenţă generală de 68,5%, ratele de infectare crescând cu vârsta, de la 65,3% în populaţia de 18-30 de ani la 88,7% la populaţia de 51-60 de ani.
Într-un studiu mai recent, care a inclus 414 pacienţi cu sindrom dispeptic, s-a identificat o rată de infectare cu H. pylori de 40,8%, mult mai mică decât cea raportată în studiile precedente.
Trebuie de asemenea observat că studiul folosit pentru compararea datelor (Sporea, 2013) a inclus o populaţie de 619 pacienţi, indiferent de prezenţa simptomelor, așadar ne-am aștepta ca un studiu condus la pacienţi simptomatici să supraevalueze prevalenţa infecţiei în populaţia generală.
Colonizarea corpului și antrului gastric este responsabilă de apariţia gastritei cronice, bolii ulceroase, gastritei atrofice cu risc crescut pentru apariţia metaplaziei intestinale, a adenocarcinomului gastric (prin carcinogeneză etapizată, de la gastrită cronică, gastrită atrofică, metaplazie intestinală, la adenocarcinom gastric) sau a limfomului MALT (mucosa-associated lymphoid tissue, ţesut limfoid asociat mucoasei).
De asemenea, dispepsia este adeseori asociată cu infecţia cu H. pylori. Prevalenţa dispepsiei funcţionale în populaţia generală este de 10-20%, fiind de obicei caracterizată de greaţă și durere epigastrică.
În Consensul de la Kyoto se diferenţiază dispepsia funcţională de dispepsia indusă de H. pylori, fiind propuși și algoritmi de diagnostic pentru această nouă entitate. Beneficiul eradicării infecţiei la această ultimă categorie de pacienţi rămâne însă controversat.
Eradicarea infecţiei cu H. pylori vindecă gastrita și poate preveni apariţia complicaţiilor pe termen lung. Astfel, ultimul Consens Maastricht (V) consideră gastrita H. pylori o boală infecţioasă indiferent de prezenţa simptomelor și de stadiul de evoluţie a bolii.
În ţările cu o incidenţă crescută a cancerului gastric a început implementarea programelor de screening populaţionale. Conform celor mai recente dovezi, se recomandă o atitudine proactivă în politicile de testare și tratament pentru H. pylori, inclusiv extinderea testării la membrii familiei pacienţilor infectaţi, precum și la populaţiile cu risc crescut (de exemplu, imigranţi din ţări cu prevalenţă mare a infecţiei).
Indicaţia de testare și eradicare a infecţiei în cazul depistării acesteia este fermă în următoarele situaţii:
Există două strategii propuse în Consensul Maastricht V:
1. Strategia „test-and-treat”, care presupune testarea pacienţilor cu dispepsie cu teste non-invazive. Este preferabilă prescrierii per primam a tratamentului simptomatic cu inhibitori de pompă de protoni (IPP) sau efectuării endoscopiei digestive superioare (EDS). Această strategie presupune costuri mai mici și disconfort redus al pacientului.
2. Strategia „endoscope-and-treat” presupune testarea pacienţilor simptomatici pentru care s-a efectuat EDS cu identificarea de leziuni.
Această abordare rămâne cea recomandată în ţările cu prevalenţă scăzută (nu e cazul României), pentru pacienţii vârstnici sau în cazul simptomelor de alarmă (scădere ponderală, disfagie, sângerare gastrointestinală, anemie feriprivă, masă abdominală palpabilă).
Recomandarea primei strategii este bazată pe date ce provin din studii clinice randomizate, în care s-a arătat doar un mic beneficiu suplimentar în cazul investigării prin EDS, care are însă costuri asociate ridicate. Tot din considerente economice, unele ghiduri recomandă tratamentul empiric cu IPP dacă prevalenţa infecţiei este sub 20%, însă nu este cazul
României.
În Consensul Maastricht sunt menţionate și următoarele categorii speciale de pacienţi care sunt candidaţi pentru testare și eradicare:
Există numeroase metode directe și indirecte pentru diagnosticul infecţiei cu H. pylori, cu particularităţi în funcţie de contextul clinic.
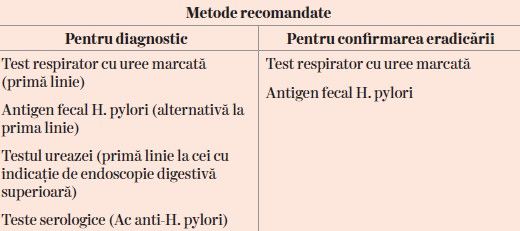
Cele mai folosite în practică sunt următoarele:
Biopsia gastrică cu examen histopatologic: metodă invazivă, ce prezintă avantajul că oferă și informaţii despre leziunile induse de infecţia cu H. pylori. La pacienţii cu tratament cronic cu IPP rezultatele pot fi fals negative. Testul ureazei este de asemenea o metodă directă, ce presupune prelevarea de biopsii.
Testul se bazează pe capacitatea H. pylori de a produce urează. Astfel, prin introducerea probei într-un mediu cu uree și un indicator de culoare, odată cu scindarea ureei în prezenţa ureazei, se va alcaliniza pH-ul soluţiei. Este metoda recomandată ca primă linie în cazul în care există indicaţie de endoscopie digestivă superioară. Are avantajul că permite iniţierea imediată a tratamentului.
Trebuie prelevate minimum două fragmente de ţesut (una din corp, una din antrul gastric). Nu se recomandă confirmarea eradicării infecţiei prin această metodă.
Metoda prezintă limite la pacienţii trataţi cu IPP, cu antibiotice, bismut sau la pacienţii cu atrofie/metaplazie importantă.
Testele serologice (determinarea anticorpilor anti-H. pylori) se bazează de obicei pe metoda ELISA și au specificitate de peste 90%. Anticorpii anti-H. pylori persistă perioade îndelungate în ser, astfel chiar și după eradicare pot exista în titru crescut. Nu se recomandă folosirea acestei metode pentru confirmarea eradicării infecţiei.
Testul respirator cu uree marcată presupune ingestia de uree marcată de către pacient, uree ce este scindată în stomac de ureaza produsă de H. pylori, urmată de eliberarea de dioxid de carbon (marcat izotopic), care este detectat și măsurat în aerul expirat.
Este metoda recomandată în primă linie atât pentru diagnostic, cât și pentru confirmarea eradicării infecţiei, având indici de performanţă excelenţi (sensibilitate 98%, specificitate 97%).
Determinarea antigenului fecal H. pylori este o metodă non-invazivă și simplă, cu performanţă similară cu testul respirator cu uree, putând fi utilizată ca alternativă.
Kiturile pentru testarea serologică rapidă, precum și testele din urină și salivă nu sunt recomandate pentru utilizarea de rutină (nici în scop diagnostic, nici pentru confirmarea eradicării).
Citiți și: Noi studii genetice și moleculare utile în tratamentele personalizate din cancerul de sân
H. pylori și rezistența la antibiotic
Material preluat din volumul „Gastroenterologie 2022” editat de „Viaţa Medicală”
Bibliografie
1. Hooi JKY, Lai WY, Ng WK, Suen MMY, Underwood FE, Tanyingoh D, Malfertheiner P, Graham DY, Wong VWS, Wu JCY, Chan FKL, Sung JJY, Kaplan GG, Ng SC. Global Prevalence of Helicobacter pylori Infection: Systematic Review and Meta-Analysis. Gastroenterology. 2017 Aug;153(2):420-429. doi: 10.1053/j.gastro.2017.04.022. Epub 2017 Apr 27. PMID: 28456631
2. Sporea I, Popescu A, van Blankenstein M, Sirli R, Focşea M, Dănilă M. The prevalence of Helicobacter pylori infection in western Romania. Rom J Gastroenterol. 2003 Mar;12(1):15-8. PMID: 12673374
3. Corojan AL, Dumitrașcu DL, Ciobanca P, Leucuta DC. Prevalence of Helicobacter pylori infection among dyspeptic patients in Northwestern Romania: A decreasing epidemiological trend in the last 30 years. Exp Ther Med. 2020;20(4):3488-3492
4. Leja M, Grinberga-Derica I, Bilgilier C, Steininger C. Review: Epidemiology of Helicobacter pylori infection. Helicobacter. 2019 Sep;24 Suppl 1:e12635
5. Eradication therapy for peptic ulcer disease in Helicobacter pylori-positive people.Ford AC, Gurusamy KS, Delaney B, Forman D, Moayyedi P Cochrane Database Syst Rev. 2016 Apr 19; 4:CD003840
6. Mladenova I. Clinical Relevance of Helicobacter pylori Infection. J Clin Med. 2021;10(16):3473. Published 2021 Aug 6. doi:10.3390/jcm10163473
7. Sugano K, Tack J, Kuipers EJ, et al. Kyoto global consensus report on Helicobacter pylori gastritis. Gut 2015;64:1353–67
8. Malfertheiner P, Megraud F, O'Morain CA, Gisbert JP, Kuipers EJ, Axon AT, Bazzoli F, Gasbarrini A, Atherton J, Graham DY, Hunt R, Moayyedi P, Rokkas T, Rugge M, Selgrad M, Suerbaum S, Sugano K, El-Omar EM; European Helicobacter and Microbiota Study Group and Consensus panel. Management of Helicobacter pylori infection-the Maastricht V/Florence Consensus Report. Gut. 2017 Jan;66(1):6-30
9. Lee YC, Dore MP, Graham DY. Diagnosis and Treatment of Helicobacter pylori Infection. Annu Rev Med. 2022 Jan 27;73:183-195
10. Dumitru E, Alexandrescu L, Hanu AC, Tocia C, Cozaru GC, Mitroi AF, Brînzan C, Așchie M, Dumitru IM. Genetic Antibiotic Resistance of Helicobacter pylori in South-Eastern Romania. J Gastrointestin Liver Dis. 2020 Mar 13;29(1):19-25
11. Nyssen OP, Bordin D et al; Hp-EuReg Investigators. European Registry on Helicobacter pylori management (Hp-EuReg): patterns and trends in first-line empirical eradication prescription and outcomes of 5 years and 21 533 patients. Gut. 2021 Jan;70(1):40-54
12. Sun Q, Liang X, Zheng Q, et al. High efficacy of 14-day triple therapy-based, bismuth containing quadruple therapy for initial Helicobacter pylori eradication. Helicobacter 2010;15:233–8
13. Graham DY, Lee Y-C,Wu M-S.Rational Helicobacter pylori therapy: evidence-based medicine rather than medicine-based evidence. Clin Gastroenterol Hepatol 2014;12:177–86. e173; Discussion e112-173.
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe