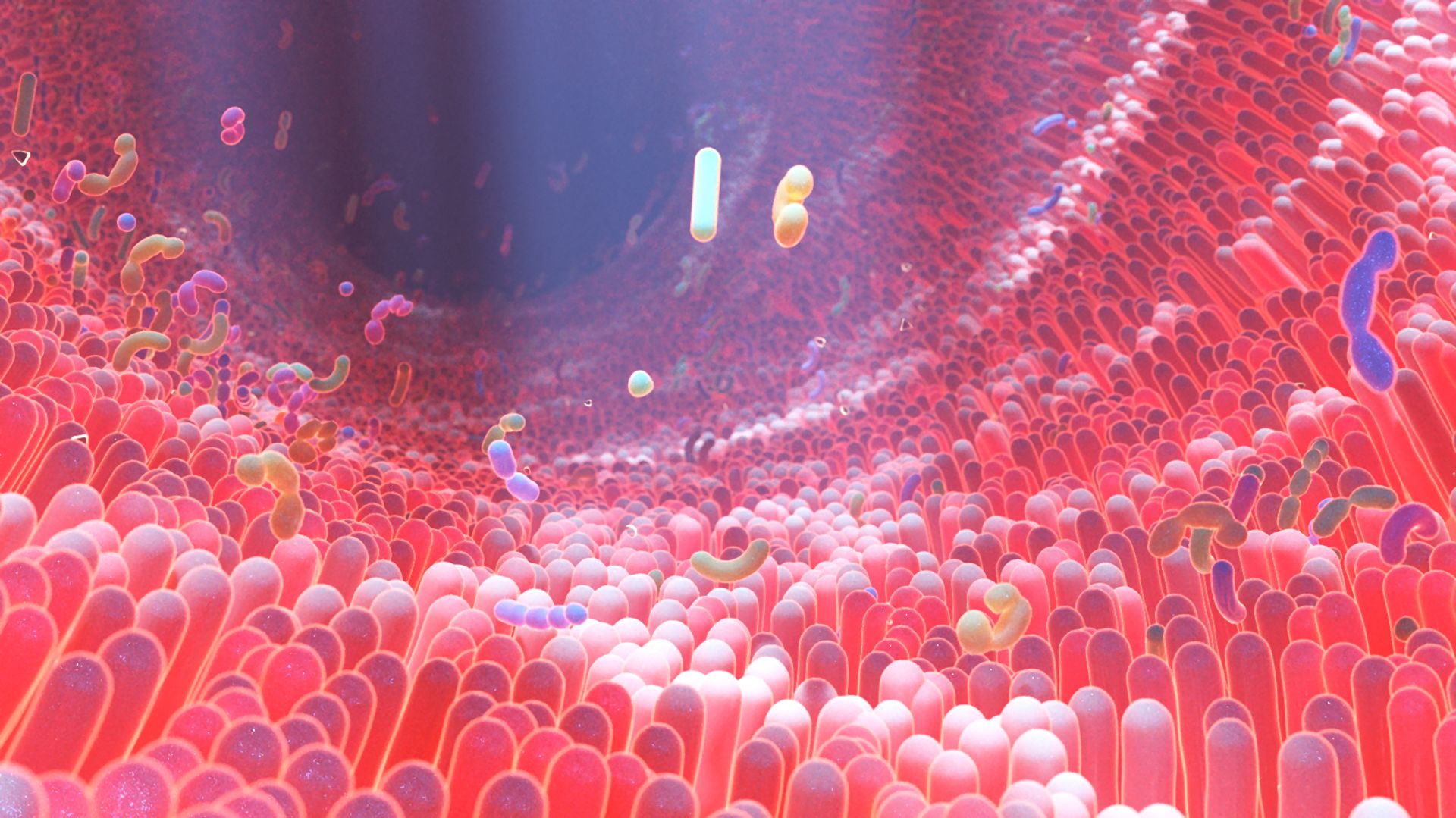
Componentele microbiomului uman au un rol important în menţinerea sănătăţii și stării de bine a organismului.
Prin termenul de microbiom se înţelege astăzi comunitatea de microorganisme care ocupă un habitat caracteristic și bine definit, având proprietăţi fizico-chimice distincte. Astfel, microbiomul nu cuprinde numai microorganismele ca atare (microbi, fungi, virusuri, protozoare, alge, archaea), ci și „teatrul lor de activitate”.
Acesta e reprezentat de constituenţii lor dezasamblaţi, de produșii de metabolism organici și anorganici ai lor și ai celulelor gazdei, ADN-ul extracelular și alte elemente genetice mobile (transpozoni, bacteriofagi, plasmide, de exemplu), încorporate în mediul unui habitat anume.
Microbiomul este un microecosistem dinamic și interactiv, integrat într-un macroecosistem cuprinzând și celulele eucariote ale gazdei, la a cărei sănătate și bună funcţionare contribuie semnificativ. Deși folosiţi frecvent ca sinonime, termenii microbiom și microbiotă au semnificaţii diferite, în sensul ca microbiota se referă doar la comunitatea microorganismelor vii existentă într-un mediu definit.
Microbiomul este un segment important al biosferei, constituind o entitate – microbiomul planetar – care contribuie semnificativ la sănătatea naturală a planetei. Conștientizarea importanţei acestui domeniu a declanșat o adevărată „revoluţie” în lumea știinţifică, materializată printr-un interes amplu și în creștere rapidă al cercetărilor.
Ca parte a microbiomului planetar și interconectat cu componentele acestuia, microbiomul uman a devenit în ultimul deceniu o preocupare de seamă nu numai a lumii știinţifice biomedicale, dar și a publicului larg, în special datorită perspectivei promiţătoare de a fi elucidate mecanismele unor boli și de a fi descoperite noi tratamente. Domeniul a evoluat rapid, ajungând în această perioadă la un volum al investiţiilor de
1,7 miliarde de dolari.
Microbiomul uman constă din imensa multitudine de microorganisme comensale și patogene ce populează suprafaţa cutaneo-mucoasă a corpului, tractul digestiv, respirator și urogenital, cea mai mare concentraţie fiind la nivelul intestinului. Ca o ilustrare, microbiomul intestinal conţine peste 100 de trilioane de bacterii din 1.000 de specii, furnizează un material genomic de 100 de ori mai mare decât întregul genom al organismului și un imens material proteic, ce conţine antigene care stimulează reacţii imune locale și generale (Figura 1).
Analiza compoziţiei microbiomului, atât în scop de cercetare, cât și de diagnostic, este realizată astăzi printr-o serie de metode avansate de biologie moleculară, grupate sub denumirea generică de „secvenţiere metagenomică”, bazate în esenţă pe reacţia polimerizării în lanţ (PCR) și a secvenţierii de nouă generaţie (NGS). Aceste metode permit o identificare mai rapidă, mai simplă și mai precisă a speciilor microbiene și a repertoriului lor funcţional într-o probă biologică obţinută din mediul lor natural, eliminându-se astfel metodele laborioase de izolare și identificare prin cultivare.
Aflate într-un complex echilibru dinamic atât între ele, cât și cu organul-gazdă, cu care se află în simbioză, precum și cu mediul înconjurător, componentele microbiomului uman au un rol important în menţinerea sănătăţii și stării de bine a organismului, microbiomul fiind considerat de unii cercetători ca un alt organ al corpului uman.
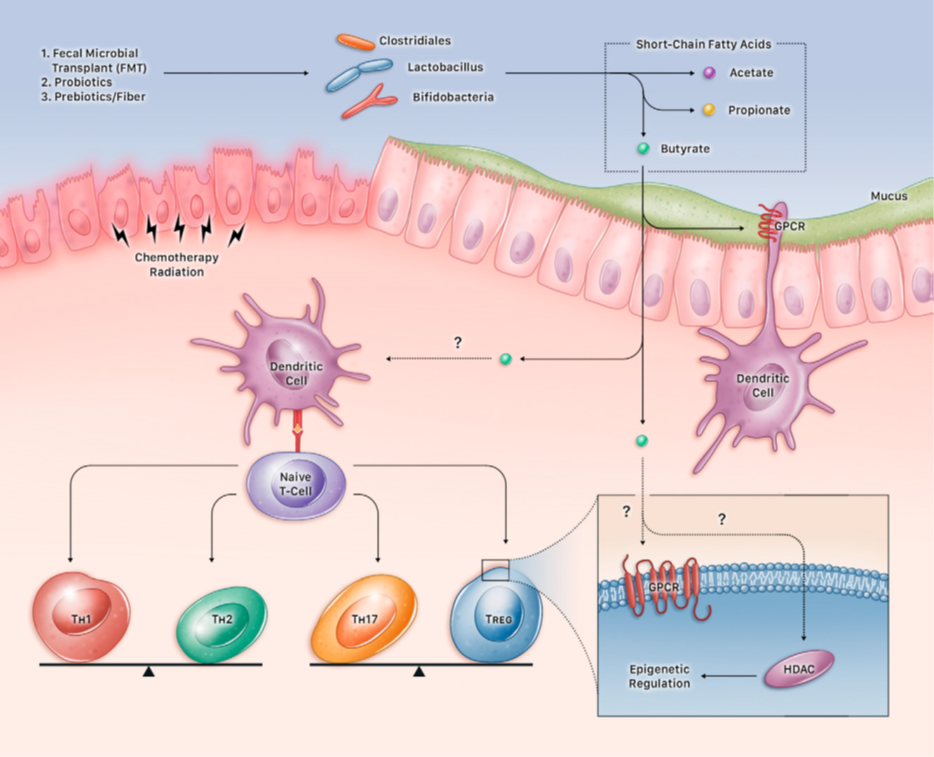
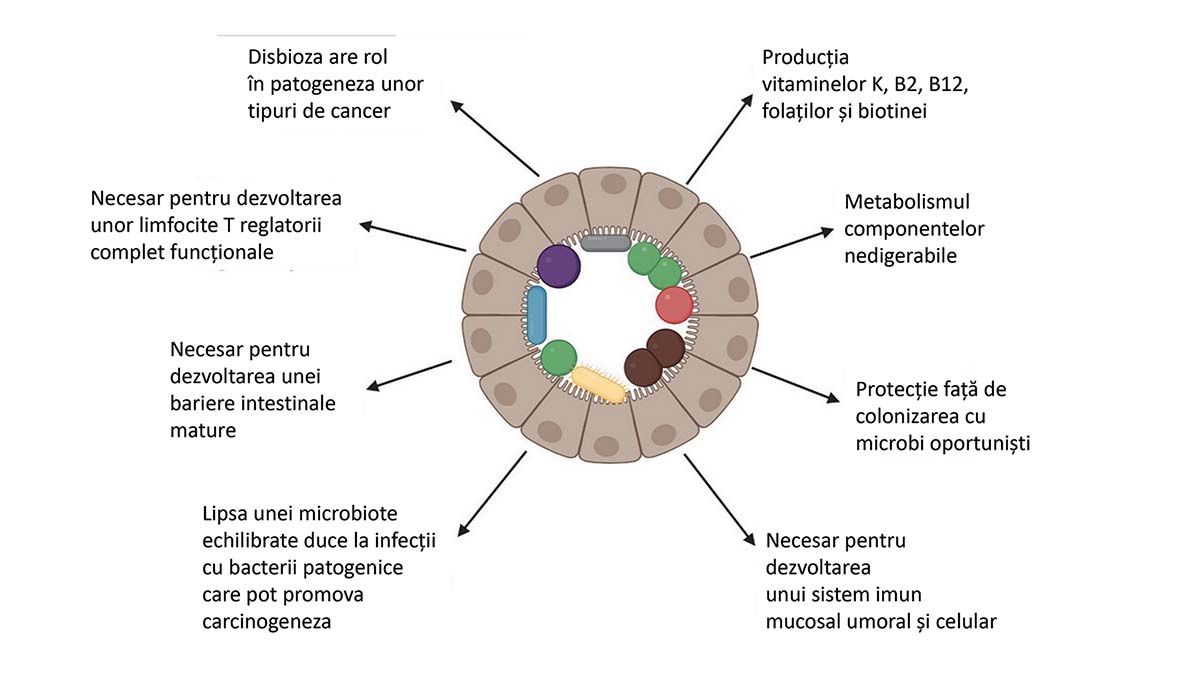
Relaţia dintre gazdă și microbiotă este simbiotică, gazda furnizând habitatul vital pentru microorganism, iar componentele microbiotei contribuind la sănătatea gazdei prin sinteza de aminoacizi esenţiali, de acizi grași cu lanţ scurt și a unor vitamine, precum și prin modelarea sistemului imun. O sinteză a principalelor efecte benefice ale microbiomului intestinal este ilustrată în figura 2 (5).
Dereglările microbiomului, reunite sub termenul de disbioză, sunt considerate în prezent ca aflându-se la originea a variate stări patologice, precum boli neurodegenerative, ateroscleroză, obezitate, diabet, cancer, boli inflamatorii intestinale.
Datele acumulate susţin implicarea diverșilor compuși ai microbiomului, îndeosebi a lipopolizaharidelor, în activitatea hematopoiezei normale, atât la nivelul stimulării progenitorilor, cât și la cel al maturării, în special a granulocitelor.
O serie de studii efectuate cu precădere în ultima decadă au sugerat implicarea microbiomului în patogeneza, evoluţia clinică și răspunsul la tratament al unor boli hematologice, îndeosebi al hemopatiilor maligne, influenţând și eficacitatea și toxicitatea chimio-, imuno- și radioterapiei, precum și riscul apariţiei și severităţii bolii grefă-contra-gazdă (BGcG) post-transplant medular (TM), cu un efect semnificativ asupra supravieţuirii în ansamblu a pacienţilor.
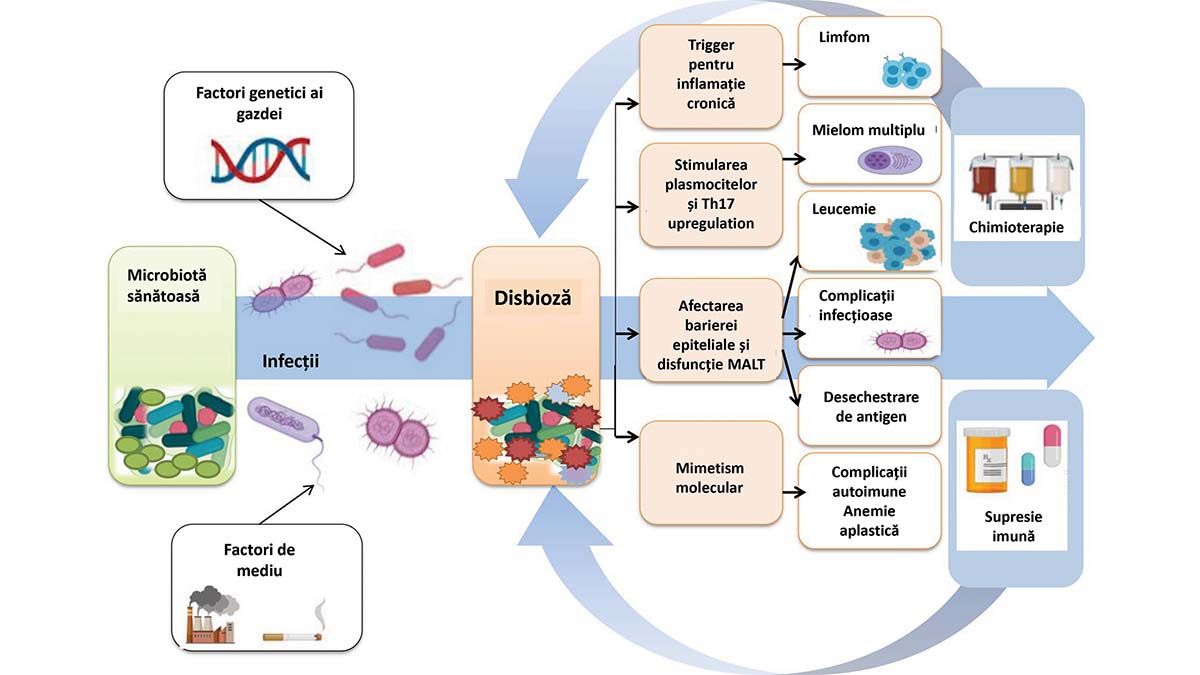
O sinteză ilustrată a posibilelor implicări ale microbiomului în acest grup de boli este prezentată în figura 3.
Fig. 3. Sinteză ilustrativă a implicării modificărilor microbiomului în bolile hematologice. Reprodus din (5)
Fără a intra în complexitatea datelor și a ipotezelor emise, câteva exemple mai convingător documentate merită a fi prezentate.
O metodă promiţătoare pentru refacerea diversităţii microbiomului intestinal după efectuarea TM și pentru ameliorarea manifestărilor intestinale ale BGcG acută, dar și a mucozitei gastrointestinale post-terapie de condiţionare mieloablativă, a fost cea a transplantului de microbiotă fecală (TMF).
Acesta constă în introducerea pe diverse căi în tractul gastrointestinal al primitorului de capsule conţinând suspensii de materii fecale de la donatori selecţionaţi. TMF este aprobat din 2014, însă doar pentru tratamentul infecţiei cronice recidivante cu Clostridioides difficile.
El face în continuare obiectul unor aplicaţii investigaţionale în diverse condiţii patologice. Cu toată amploarea lor, cercetările privind microbiomul uman în general și interrelaţia dintre acesta și bolile hematologice în special, cât și aplicaţiile terapeutice se află la început. Standardizarea metodologiei de studiu și îmbunătăţirea alcătuirii trialurilor odată cu extinderea numărului acestora sunt premise necesare pentru o medicină de precizie și în acest domeniu.
S-a dovedit că o bună parte din complicaţiile alotransplantului
(alo-TM) sunt consecinţa scăderii semnificative a diversităţii microbiotei
intestinale. Această scădere este graduală pe parcursul
procedurii, fiind determinată de o combinaţie de factori precum tratamentul de condiţionare, tratamentul antibiotic, modificările dietei,
inflamaţia intestinală.
Se asociază cu o modificare a compoziţiei în sensul reducerii genurilor comensale și creșterii celor potenţial patogene. O analiză a microbiomului intestinal, dar și a celui gingivo-dentar, nazofaringian ș.a. înainte de alo-TM este astăzi o practică uzuală, pentru identificarea atât a unor specii patogene, cât și a disbiozei, care s-a dovedit a fi un factor predictiv de mortalitate independent la pacienţii transplantaţi.
S-a emis ipoteza că lipopolizaharidele originare din bacteriile
Gram-negative intestinale traversează bariera mucoasei afectate
de regimul de condiţionare (permeabilitate crescută, strat de mucus
redus, secreţie redusă de defensine) și stimulează eliberarea de
citokine proinflamatorii care mediază BGcG acută, complicaţie cu
potenţial letal a TM.
Dominaţia speciilor Enterococcus, Escherichia coli sau Prevotella s-a asociat cu o incidenţă și o severitate crescută ale BGcG, în timp ce cantităţi crescute de microorganisme din genul Blautia sau Clostridiales au fost asociate cu o mortalitate mai redusă prin BGcG acută și cu o supravieţuire mai lungă post-TM.
Limfomul gastric tip MALT (mucosa-associated lymphoid tissue), cu originea în ţesutul limfatic adiacent mucoasei gastrice, este asociat etiopatogenic cu inflamaţia cronică indusă de infecţia cu Helicobacter pylori, fapt susţinut de dovezi epidemiologice, anatomopatologice, bacteriologice și clinice.
Simpla eradicare cu antibiotice a acestei infecţii este urmată de regresia limfomului la 60-90% din cazuri, iar recrudescenţa infecţiei se însoţește de reapariţia tumorii.
Citiți și: Diagnosticul hematologic al anemiilor la vârstnici
Bibliografie
1. Severyn C.J. et al. Microbiota modification in hematology: still at the bench or ready for the bedside. Blood Adv 2019, 3(21);3461
2. Berg G. et al. Microbiome definition re-visited: old concepts and new challenges. Microbiome 2020, 8:103
3. Theilgaard-M ̈onch K. Gut microbiota sustains hematopoiesis. Blood,2017,129(6): 662
4. Prescott S.L. History of medicine: Origin of the term microbiome and why it matters. Human Microbiome Journal 2017, 4:24-25
5. Fattizzo B. et al. Recent insights into the role of the microbiome in malignant and benign hematologic diseases. Critical Reviews in Oncology / Hematology doi.org/10.1016/j.critrevonc.2021.103289
6. Allegra A. et al. Role of the microbiota in hematologic malignancies. The Netherlands Journal of Medicine 2019,77(2):67
7. Nogrady B. How gut reactions are shaping cancer treatment. Nature News 2022, 06.04.
8. Uribe-Herranz M. et all. Gut microbiota influence in hematological malignancies: from genesis to cure. Int J Mol Sci. 2021;22(3):1026
9. Staffas A. et al. The intestinal microbiota in allogeneic hematopoietic cell transplant and graft-versus-host disease. Blood. 2017;129(8):927
10. Yan H, Baldridge MT, King KY. Hematopoiesis and the bacterial microbiome. Blood 2018;132(6):559
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe